
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl—,消耗等物质的量浓度的AgNO3溶液的体积比为3:2:1,则上述溶液的体积比为( )
A.1:1:1 B.3:2:1 C.6:3:2 D.9:3:1
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
下列各组离子在碱性条件下能大量共存,而在强酸性条件下能发生氧化还原反应的( )
A.Mg2+、Na+、SO42-、Cl— B.K+、CO32-、Cl—、NO3—
C.Na+、K+、NO3—、SO32— D.NH4+、Na+、SO42-、NO3—
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
下列离子方程式正确的是( )
A.Ba(OH)2与KAl(SO4)2·12H2O溶液混合生成沉淀质量最大
2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2- +2H2O
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C.H218O中投入Na2O2固体:2H218O+2O22-=4OH-+18O2↑
D.CuCl2溶液中加入NaHS溶液:Cu2++2HS-+2H2O=Cu(OH)2↓+2H2S↑
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
在硫酸铜溶液中加入碘化钾溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析证明白色沉淀是碘化亚铜.则能正确表示这个氧化还原反应的离子方程式( )
A.Cu2++3I-====CuI↓+I2 B.Cu2++2I-====Cu++I2
C.2Cu2++2I-====2Cu++I2 D.2Cu2++4I-====2CuI↓+I2
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
已知氯化铁溶液能与碘化钾反应生成氯化亚铁、氯化钾和碘单质.某溶液中含有的溶质是FeBr2、FeI2,若向该溶液中通入一定量的氯气,再向反应后的溶液中滴加KSCN溶液,结果溶液变成血红色,则下列叙述正确的是( )
①原溶液中的Br-一定被氧化
②通入氯气后原溶液中的Fe2+一定被氧化;
③不能确定通入氯气之后的溶液中是否存在Fe2+;
④若取少量所得溶液,再加入 CCl4,振荡、静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中的Fe2+、Br-、I-均被完全氧化
A.只有②③ B.只有②③④ C.只有①④ D.①②③④
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
相同物质的量的下列溶液中的溶质,充分吸收同状况的SO2,吸收体积最大的是( )
A.高锰酸钾(H+) B.碳酸钠 C.溴 D.氢氧化钡
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
将1mol/L硝酸溶液逐滴加入某合金(仅含铜、铁)中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法不正确的是( )
A.若金属有剩余,则剩余金属一定含Cu .
B.若硝酸溶液体积为100ml,反应后金属有剩余,则可计算产生NO的物质的量.
C.若金属恰好全部溶解后,再加硝酸溶液仍能产生NO.
D.若金属全部溶解,则溶液中一定含Fe3+、Cu2+.
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
把一块镁铝合金投入到1 mol·L-1 盐酸中,待合金完全溶解后,再往溶液里加入1 mol·L-1 NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如右图所示.下列说法中错误的是( )
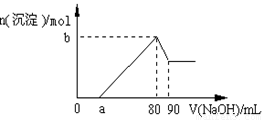
A.盐酸的体积为80 mL B.a的取值范围为0 < a<50
C.n (Mg2+) < 0. 025 mol D.当a值为30时,b值为0.01
查看答案和解析>>
科目: 来源:2011-2012学年江西省高三上学期期中考试化学试卷 题型:选择题
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2 .在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如右图所示.下列说法正确的是( )
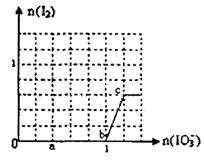
A.反应过程中的氧化产物均为SO3
B.a点时剩余NaHSO3的物质的量为1.8 mol
C.c点时的还原产物可能是KI或NaI
D.当溶液中I¯与I2的物质的量之比为1:1时,加入的KIO3为1.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com