
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:填空题
(12分)工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝。工艺流程如右图:
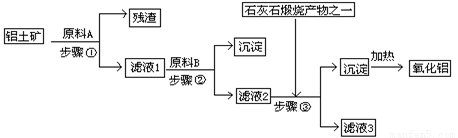
(1) 原料A的名称是____,步骤①反应的离子方程式是_________________。
(2) 滤液1中要加入稍过量原料B,原料B的化学式是__,步骤②反应的离子方程式是
(3) 步骤③的化学方程式是:_____________________________________________。
(4) 如果省去步骤①,即溶解铝土矿是从加入原料B开始,后续操作不变,则会对氧化铝的提取有什么影响__________________________________________________。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:实验题
(12分)硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:

已知几种盐的溶解度随温度变化的曲线如右图所示:

回答下列问题:
(1)酸浸、过滤后滤液中的金属阳离子是________________。
(2)煅烧FeCO3生成产品I的化学反应方程式为________________________________。
实验室进行煅烧操作所需仪器除了酒精喷灯、泥三角、三脚架、玻璃棒外,还有__________。
(3)产品Ⅱ的化学式为_______________,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是: 。
(4)检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,
查看答案和解析>>
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:填空题
(12分) 由短周期元素组成的10种物质A~J间有下图所示的转化关系。
已知A、B为同周期相邻元素的单质,其余均为化合物;通常状况下A为固体,B、D为气体,F为液体;A和G的浓溶液加热时反应生成D和F;J在光照时有I生成。
试回答:
(1)写出下列物质的化学式:B_________,E__________,F的结构式__________。
(2)反应①的离子方程式为______________________________;
(3)足量铁与G的热的浓溶液反应所得气体是___;铁与B反应的化学方程式__________。
(4)C是一种重要的化工产品,为易挥发的樱桃红色液体。若反应②中生成的G、A和I的物质的量之比为1︰2︰6,则C的电子式为_____,反应②的化学方程式为_____。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:实验题
(12分)高铁酸钾是一种高效的多功能的水处理剂。工业上常采用NaClO氧化法生产,原理为:3NaClO + 2Fe(NO3)3 + 10NaOH=2Na2FeO4↓+ 3NaCl + 6NaNO3 + 5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH主要的生产流程如下:
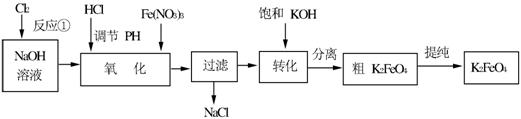
(1)写出反应①的离子方程式 。
(2)流程图中“转化”是在某低温下进行的,说明此温度下Ksp(K2FeO4) Ksp(Na2FeO4)(填“>”或“<”或“=”)。
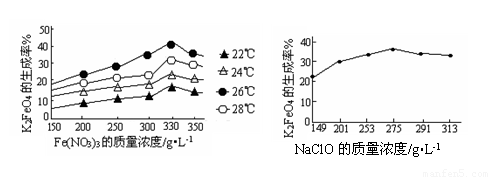
(3)反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。
上左图为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;
右图为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。
①工业生产中最佳温度为 ℃,此时Fe(NO3)3与NaClO两种溶液最佳质量浓度之比为 。
②若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
。
若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式: 。
(4)K2FeO4
在水溶液中易水解:4FeO42—+10H2O 4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)。
4Fe(OH)3+8OH—+3O2↑。在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 溶液(填序号)。
A.H2O B.CH3COONa、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
查看答案和解析>>
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:计算题
(8分)某研究性学习小组用48.0克铜屑与氧化铜的混合物与硫酸和硝酸的混酸100 ml溶液反应制取五水硫酸铜晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后溶液中只有硫酸铜。若在固体混合物中铜屑的质量分数为0.4,试计算:(1)最终制得晶体的质量。(2)混酸中两溶质的物质的量浓度。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省苏州市高三上学期10月份月考化学试卷 题型:填空题
(12分) 下图所示为血红蛋白和肌红蛋白的活性部分――血红素的结构式。
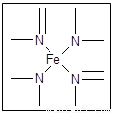
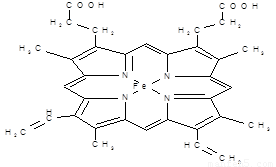
血红素的结构式
回答下列问题:
⑴血红素中含有C、H、O、N、Fe五种元素,C、N、O三种元素的第一电离能由小到大的顺序是 ,写出基态Fe原子的核外电子排布式 。
⑵血红素中N原子的杂化方式为 ,在右图的方框内用“→”标出Fe2+的配位键。
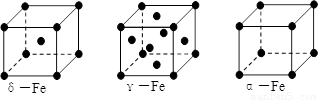
⑶铁有δ、γ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为 ,δ、α两种晶胞中铁原子的配位数之比为 。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三下学期开学质量检测化学试卷 题型:选择题
从化学角度分析,下列叙述不正确的是
A.利用太阳能蒸馏海水是海水淡化的方法之一
B.将地沟油回收再加工为食用油,以减缓水体富营养化
C.研制开发燃料电池汽车,降低机动车尾气污染,可以减少PM2.5污染
D.绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三下学期开学质量检测化学试卷 题型:选择题
下列有关化学用语,表达正确的是
A.Na2S的电子式: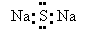 B.铯—137:137Cs
B.铯—137:137Cs
C.O2―的结构示意图: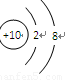 D.乙烯分子的球棍模型:
D.乙烯分子的球棍模型: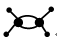
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三下学期开学质量检测化学试卷 题型:选择题
下列有关物质的性质及其应用均正确的是
A.NH3溶于水后显碱性,在FeC13饱和溶液中通入适量NH3可制取Fe(OH)3胶体
B.金属有导热性,钾、钠熔点不高,核反应堆内使用液体钾钠合金作载热介质
C.碳酸钠溶液显碱性,用热的饱和碳酸钠溶液可除去金属表面的矿物油污
D.次氯酸钠具有强还原性,可用于配制“84”消毒液
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三下学期开学质量检测化学试卷 题型:选择题
室温下,下列各组离子在指定溶液中一定能大量共存的是
A.饱和氯水中:Cl-、NO3-、Na+ 、SO32-
B.c(H+)=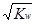 的溶液中:K+、Fe3+ 、Cl-、SO42-
的溶液中:K+、Fe3+ 、Cl-、SO42-
C.澄清透明的溶液中:Cu2+、NH4+、NO3—、ClO4—
D.使红色石蕊试纸变蓝的溶液中:CH3COO-、HCO3-、Na+、K+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com