
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:选择题
CPAE是蜂胶的主要活性成分,也可由咖啡酸合成:
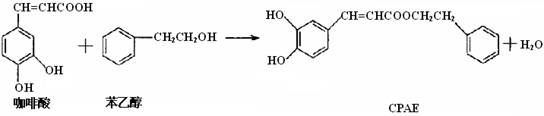
下列说法不正确的是
A.咖啡酸分子中所有原子可能处在同一个平面上
B.可用金属Na检测上述反应是否残留苯乙醇
C.1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:选择题
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)  Si(s)+4HCl(g)
△H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器中进行以上的反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g)
△H=+QkJ·mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器中进行以上的反应(此条件下为可逆反应),下列叙述正确的是
A.反应过程中,若增大压强能提高SiCl4的转化率
B.当反应吸热为0.025QkJ时,生成的HCl与100mL1mol·L-1的NaOH溶液恰好反应
C.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
D. 若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:选择题
某弱酸的酸式盐有NaH2XO4和Na2HXO4,其中NaH2XO4溶液呈酸性,Na2HXO4溶液呈碱性。50℃时,浓度均为0.1mol•L-1NaH2XO4溶液和Na2HXO4溶液中均存在的关系是
A.c(H+)•c(OH-) > 1×10-14
B. c(Na+)+ c(H+)=c(H2XO4-)+ c(OH-)+ 2c(HXO42-)+ 3c(XO43-)
C.c(H+) + 2c(H3XO4) + c(H2XO4-) = c(XO43-) + c(OH-)
D.c(H+) + c(H3XO4)=c(HXO42-)+ 2c(XO43-)+ c(OH-)
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:选择题
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3。则下列说法正确的是
A.反应过程中,被氧化与被还原的元素的物质的量之比为2:1
B.NF3是一种无色、无臭的气体,因此NF3泄漏时常常不易被察觉]
C.一旦NF3泄漏,可以用石灰水溶液喷淋的方法减少污染
D.若反应中转移的电子数目为6.02×l023,则生成22.4L NO气体
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:选择题
可逆反应①X(g)+2Y(g) 2Z(g) 、②2M(g)
2Z(g) 、②2M(g) N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
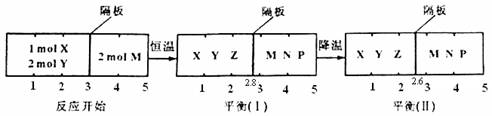
下列判断正确的是
A.反应①的正反应是吸热反应
B.达平衡(I)时体系的压强与反应开始时体系的压强之比为14:15
C.在平衡(I)和平衡(II)中M的体积分数相等
D.达平衡(I)时,X的转化率为5/11
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:实验题
(12分)硫酸亚铁铵(NH4)2SO4•FeSO4•6H2O是一种重要化学试剂,实验室用除去锌镀层的铁片来制取硫酸亚铁铵,流程如下:
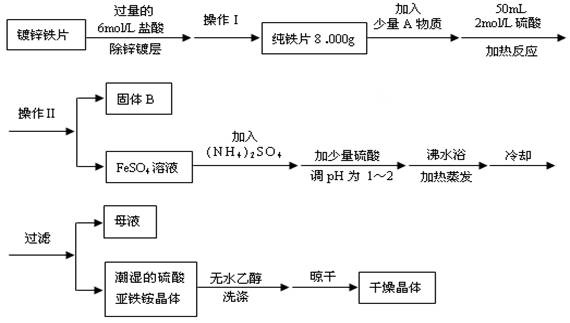
请回答下列问题:
(1)确定锌镀层被除去的标志是 ;
计算上述铁片锌镀层的厚度,不需要的数据是 (填编号)。
a.锌的密度ρ(g/cm3) b.镀锌铁片质量m 1(g) c.纯铁片质量m 2(g)
d.镀锌铁片面积S(cm2) e.镀锌铁片厚度h(cm)
(2)上述流程中:操作Ⅰ是取出铁片、 、 、称量。
(3)A物质可以为 (填编号)。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(4)用无水乙醇洗涤潮湿的硫酸亚铁铵晶体是为了除去晶体表面残留的水分,不用加热烘干的原因是 。
(5)鉴定所得晶体中含有Fe2+、NH4+、SO42-离子的实验方法正确的是 (填编号)。
a.取少量样品于试管,加水溶解,通入适量Cl2,再加KSCN溶液,观察现象
b.取少量样品于试管,加水溶解,加入NaOH溶液,露置于空气中,观察现象
c.取少量样品于试管,加水溶解,加入浓NaOH溶液并加热,用湿润的红色石蕊试纸置于试管口,观察试纸颜色的变化
d.取少量样品于试管,加水溶解,加入盐酸后再加入BaCl2溶液,观察现象
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:填空题
(16分)炔抑制剂的合成路线如下:
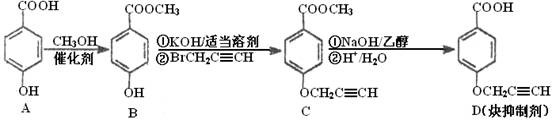 (1)化合物A核磁共振氢谱有________种峰。
(1)化合物A核磁共振氢谱有________种峰。
(2)化合物C中含氧官能团有___________、__________(填名称)。
(3)鉴别化合物B和C最适宜的试剂是________________。
(4)写出A—B的化学方程式__________________________。
(5)B的同分异构体很多,符合下列条件的异构体有______________种。
①苯的衍生物 ②含有羧基和羟基 ③分子中无甲基
(6)试以苯酚、氯乙酸钠(ClCH2COONa)、正丁醇为原料(无机试剂任用),结合题中有关信息,请补充完整的合成路线流程图。
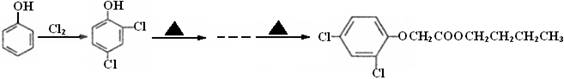
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:填空题
(12分)MnSO4·H2O在工业、农业等方面有广泛的应用。
(一)制备:工业上用化工厂尾气中低浓度SO2还原MnO2矿制备MnSO4·H2O过程如下:

已知: 常温时部分硫化物难溶盐的Ksp:CuS--6.3×10-36、PbS--1.0×10-28、NiS--2.0×10-26、MnS--2.5×10-10,请回答下列问题:
(1)生产中MnO2矿粉碎的目的是 。(2)除铁发生的离子反应方程式为 。
(3)除重金属离子后,若混合溶液中Cu2+、Pb2+、Ni2+的浓度均为1.0×10-5mol/L,则c(S2-)最大= mol/L。
(二):性质—热稳定性:MnSO4·H2O在1150℃高温下分解的产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是
(三)废水处理:工厂废水中主要污染为Mn2+和Cr6+,现研究铁屑用量和pH值对废水中铬、锰去除率的影响,(1)取100mL废水于250 mL三角瓶中,调节pH值到规定值,分别加入不同量的废铁屑.得到铁屑用量对铬和锰去除率的影响如下图1所示。则在pH一定时,废水中铁屑用量为 时锰、铬去除率最好
(2)取100mL废水于250 mL三角瓶中,加入规定量的铁粉,调成不同的pH值。得到pH值对铬和锰去除率的影响如下图2所示。则在铁屑用量一定时,废水pH= 时锰、铬去除率最好

查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:填空题
(14分) 草酸亚铁可用于合成锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)等,其制备过程主要包括:
a.将硫酸亚铁铵【(NH4)2Fe(SO4)2·6H2O】晶体溶于适量蒸馏水,加入适量稀硫酸酸化。
b.将上述溶液煮沸,逐滴加入H2C2O4溶液,直至沉淀完全。
c.静置、倾去上层清液、过滤、洗涤、50℃以下烘干。试回答下列问题:
(1)配制(NH4)2Fe(SO4)2·6H2O溶液时,需加入少量稀硫酸,目的是 。
(2)将制得的产品(FeC2O4·2H2O)在氩气气氛中进行热重分析,结果如图(TG%表示残留固体质量占原样品总质量的百分数)。
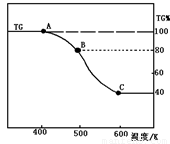
① 则A-B发生反应的化学方程式为: 。
② 精确研究表明,B-C实际是分两步进行的,每步释放一种气体,其中第一步释放的气体相对分子质量较第二步的小,试写出B-C两步反应的方程式: 、
;
(3)Li2CO3、FeC2O4·2H2O和SiO2粉末均匀混合,在800℃. 的氩气中烧结6小时,即可制成硅酸亚铁锂。①合成硅酸亚铁锂的化学方程式为: 。
②该锂电池放电时的总反应式为LiFeSiO4+Li=Li2FeSiO4,写出相应的电极反应式:
正极 、负极 。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三元月双周练习化学试卷 题型:填空题
(14分)在一个装有可移动活塞的容器中模拟传统工业合成氨的反应:N2(g)+3H2(g)
 2NH3(g),反应达到平衡后,测得NH3的物质的量为amol
2NH3(g),反应达到平衡后,测得NH3的物质的量为amol
(1)保持容器内的温度和压强不变,向平衡体系中又通入少量的H2,再次达到平衡后,测得NH3的物质的量为bmol,则 a b(填入“>”或“<”或“=”或“无法确定”,下同)。若向平衡体系中通入的是少量N2,则 a b。
煤制油是一项新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义。下列是煤通过间接液化技术制汽油和丙烯的主要工艺流程图。

已知甲醇制烃的反应原理为:

(2)为了提高原料利用率,上述工艺中应控制合成气中V(CO):V(H2)= 。
(3)由二甲醚在催化剂作用下转化为丙烯的化学方程式为: 。
(4)每生产1t甲醇约耗煤1.5t,每生产1 t汽油约需耗2.4t甲醇,2015年我国煤制油将达到1000万吨,则2015年当年需消耗原煤约 万吨。
(5)采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4 %~7%,均四甲苯的结构简式为: 。
(6)采用DMTO技术,若获得乙烯和丙烯及丁烯3种烃,生成丁烯的选择性(转化丁烯的甲醇的物质的量与甲醇总物质的量之比)为20%,其余生成乙烯和丙烯,设丙烯的选择性为x,今有403.2L(标准状况)合成气,且完全转化为甲醇,甲醇转化为烯烃的总转化率亦为100%,请作出丙烯的物质的量随x变化的曲线。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com