
科目: 来源:2011-2012学年江苏省高三上学期期中考试化学试卷 题型:实验题
(12分) 从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:

方案乙:

(1)两个方案中,符合当前生产中绿色化学理念的是方案 ,理由是 。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________________,
若不考虑绿色化学要求,溶解铜生成硫酸铜时,还可将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使铜溶解完全,则理论上硫酸和硝酸的物质的量之比最佳为: ︰ 。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a—1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。
通过计算测知该晶体的化学式是 。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3 = 2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol·L-1 FeCl3 溶液中,待样品完全溶解后,加水20mL,用0.1000mol·L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:
Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+ = Fe 3+ + Ce3+
通过计算说明上述样品中CuCl的质量分数是否符合标准。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期期中考试化学试卷 题型:实验题
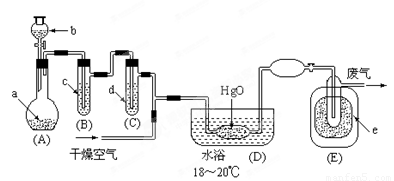
(15分)氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液.制备出之后要冷却为固态才便于操作和贮存。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,铁架台和夹持仪器已略去。
部分物质的有关物理数据如下:?
|
化学式 |
熔点(单位:℃) |
沸点(单位:℃) |
|
N2 |
-209.86 |
-195.8 |
|
O2 |
-218.4 |
-183 |
|
CO2 |
-57 |
/ |
|
NH3 |
-77.3 |
-33.35 |
|
Cl2 |
-101 |
-34.6 |
试回答:?
(1)A中盛有深色固体试剂a是 ,分液漏斗中b试剂是 。
(2)B中盛有液体c是 ,C中的液体d是 。?
(3)D中发生化学反应的化学方程式是 。
(4)E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是 。
(5)装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是 ,用这些不同的连接方式的主要理由是 。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期期中考试化学试卷 题型:填空题
(14分)氟和氟盐是化工原料。由于氟气性质活泼,很晚才制取出来。
(1)不能通过电解纯净的液态HF获得F2,其原因是 ;但电解液态KHF2时,两极分别得到F2和H2,写出阳极上HF2- 放电产生气体的电极反应式 。
(2)利用K2MnF6和SbF5在一定条件下发生反应也能制取氟,同时生成KSbF6 和MnF3,化学方程式为 ,其中还原产物是 。
(3)已知氟化氢气体中存在下列平衡 :H3F3 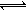 3HF △H >0, H2F2
3HF △H >0, H2F2 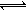 2HF △H >0。
2HF △H >0。
①若在定温定容条件下再充入H3F3,则H3F3与HF的浓度(mol/L)比值 (填“增大”“减小”或“不变”,下同);
②若在定温定容条件下再充入HF,则H3F3与HF 的浓度(mol/L)比值 。
(4)一定浓度的HF和Al2(SO4)3混合液中,铝的 各种微粒含量ƒ随pH的分布曲线如图示。用NaOH使混合液的pH从5调整到7,写出有关反应的离子方程式为
。

查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期期中考试化学试卷 题型:填空题
(12分
下图是元素周期表的一部分:

⑴表中区域名称s、p……等确定的依据是_______________________________________。
⑵已知A原子的M层和N层的电子数分别比B原子的M层和N层的电子数少7个和4个,则A的核外电子排布式为______________,B在元素周期表中的位置是___________。
⑶上表中元素x的一种氢化物的晶体结构如图所示,写出该化合物在氯气中燃烧的化学方程式 。

除x外,第四周期中最外层只有一个电子的还有 (填元素名称)。
⑷表中短周期非金属元素之间可以形成形形色色的有机物,如邻羟基苯甲醛( )和对羟基苯甲醛(
)和对羟基苯甲醛( ),前者沸点低于后者,理由是
),前者沸点低于后者,理由是
_____ 。
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
“化学,我们的生活,我们的未来”是2011年“国际化学年”的主题。你认为下列行为中,不符合这一主题的是
A.控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源
B.研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展
C.开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料
D.实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle)
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
下列化学用语的理解正确的是
A.离子结构示意图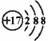 可以表示35Cl-,也可以表示37Cl-
可以表示35Cl-,也可以表示37Cl-
B.电子式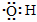 :可以表示羟基,也可以表示氢氧根离子
:可以表示羟基,也可以表示氢氧根离子
C.比例模型 :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
D.结构简式(CH3)2CHOH:可以表示1–丙醇,也可以表示2–丙醇
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是

A.原溶液中一定含有SO42-离子 B.原溶液中一定含有NH4+离子
C.原溶液中一定含有Cl-离子 D.原溶液中一定含有Fe3+离子
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
下列各组离子在指定溶液中能大量共存的是
①常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
②加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-
③中性溶液:Fe3+、Al3+、NO3-、SO42-
④使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-
⑤无色溶液中:K+、AlO2-、NO3-、HCO3-
A.②③ B.①③ C.① D.①④⑤
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
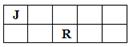
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是
A.J和氢组成的化合物分子有多种
B.工业上不用电解M和T组成的化合物来制备M
C.R、T两元素的气态氢化物中,R的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
查看答案和解析>>
科目: 来源:2011-2012学年江苏省高三上学期第二次月考化学试卷 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.漂白粉露置在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
B.向滴有酚酞的硅酸钠溶液中边加边振荡地滴加盐酸至红色变浅并接近消失:
2H++SiO32-=H2SiO3(胶体)
C.向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+Fe(OH)3= FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com