
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
X、Y、Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是
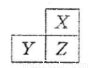
A.原子半径: Y >Z >X
B.气态氢化物的热稳定性:X<Z
C.Y和Z的最高价氧化物对应水化物均为强酸
D.若Z的最高正价为+m,则X的最高正价也一定为+m
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
下列各组离子,一定能在指定环境中大量共存的是 ( )
A.在含有大量I-离子的溶液中:Cl¯、Fe3+、Al3+、Cu2+
B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存
C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯
D.在加入Al能放出大量H2的溶液中:NH4+、SO42¯ 、C1¯、HCO3¯
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
下列有关以KOH溶液为电解液的氢氧燃料电池的叙述不正确的是
A.正极反应式为:O2 + 2H2O +4e- =4OH-
B.工作一段时间后,电解液中KOH的物质的量浓度不变
C.该燃料电池的总反应式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
关于下列各装置图的叙述中,正确的是
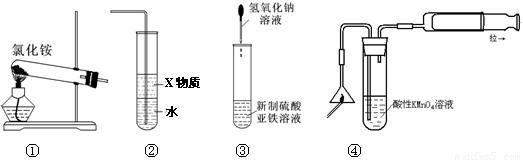
A.实验室用装置①制取氨气
B.装置②中X若为苯,可用于吸收氨气,并防止倒吸
C.装置③可用于制备氢氧化亚铁并观察其颜色
D.装置④可用于检验火柴头燃烧产生的SO2
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
下列说法正确的是
A. Na和Cs属于第IA族元素,Cs失去电子能力比Na强
B.Na2O2与水反应、红热的Fe与水蒸气反应均能反应生成碱
C.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
D.镁条在空气中燃烧生成的氧化物是MgO,钠在空气中燃烧生成的氧化物是Na2O2
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:选择题
下列说法正确的是
A.常温下pH为5的盐酸溶液稀释1000倍后,pH等于8
B.浓度均为0.1mol/L的氨水和氯化铵溶液,水电离出的c(H+)前者小于后者
C.碳酸钠溶液中存在:c(Na+) =2c(CO32-) +c(HCO3-)+c(H2CO3)
D.等物质的量浓度的CH3COOH溶液与KOH溶液任意比混合:c(K+) +c(H+) =c(OH-) +c(CH3COO-)
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:填空题
(16分)从樟科植物枝叶提取的精油中含有甲、乙两种成分:

(1) ①甲和乙中含氧官能团的名称分别为 和 。
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液显呈现紫色
(2) 由甲转化为乙的过程为(已略去无关产物):

反应I的反应类型为 ,Y的结构简式 。
(3) 1mol乙最多可与 mol H2发生加成反应。
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:填空题
(16分)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。

请回答下列问题:
(1)在“图1”中,曲线 (填:a或b)表示使用了催化剂;该反应属于 (填:吸热、放热)反应。
(2)下列说法正确的是
A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会减小
(3)从反应开始到建立平衡, v(H2)=____
____ ;该温度下CO(g)+2H2(g)
 CH3OH(g)的化学平衡常数为______________ 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____ (填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为______________ 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____ (填“增大”、“减小”或“不变”)。
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(5)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:填空题
(16分)炼锌厂产生的工业废渣——锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4·7H2O和金属镉是一个有益的尝试,其流程如下:
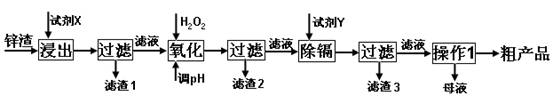
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7;锌的金属活动性比镉强。
试回答下列问题:
(1)“浸出”时用到的“试剂X”为 (填名称)。
(2)写出“氧化”过程的离子方程式 。
(3)“调pH”过程可以选用 。(从以下选项选择, 填序号)
A.H2SO4 B.ZnO C.NaOH
“滤渣2”的主要成分是 (填化学式,下同)。
(4)“试剂Y”是______________;“滤渣3”的成分为______________________。
(5)“操作1”的方法是___ ____;在“操作1”时,必须采取的实验措施是 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省潮汕两市名校高三上学期期中联考理综试题(化学部分) 题型:实验题
(16分) I、实验室中常以BaSO4重量法测定BaCl2·nH2O中的Ba的含量主要步骤如下:
① 灼烧瓷坩埚至恒重,称得坩埚的质量
② 称取BaCl2·nH2O并在烧杯中溶解,加盐酸处理
③ 将一定浓度的过量硫酸滴入钡盐中得到白色沉淀
④ 静置,
⑤ 将沉淀和滤纸置于瓷坩埚中,经酒精喷灯加热碳化后,继续在800-850℃灼烧至恒重,称重
⑥ 计算
请回答下列问题:
(1)省略第①步中“灼烧瓷坩埚至恒重”可能导致计算结果_______(填“偏高”、“不变”或“偏低”)。
(2)第④步静置后的操作是 。
(3)第⑤步灼烧温度不超过900℃,是因为_______________________。
II、某同学用氨水吸收一定量的SO2,吸收后溶液中可能含有OH-、SO32-、SO42-、 HSO3- 等阴离子中的若干种。
(4)写出氨水吸收过量SO2的反应的离子方程式:
(5)已知亚硫酸氢盐一般可溶于水。仅限选择的仪器和试剂:烧杯、试管、玻璃棒、胶头滴管; 2 mol/L盐酸、2 mol/L硝酸、1 mol/L氯化钡溶液、l mol/L氢氧化钡溶液、品红溶液、蒸馏水。请设计实验探究吸收后溶液中是否存在SO32-、HSO3-,将实验操作、预期的实验现象和结论填在下表中。
|
实验操作 |
预期现象与结论 |
|
步骤1:取少量待测液放入试管1中,滴加过量lmol/L氯化钡溶液。 |
若不出现浑浊,则溶液中不存在SO32-, 若出现浑浊,则溶液中可能含有SO32-。 |
|
步骤2:若出现浑浊,静置一段时间后,将上层清液倒入试管2中。往试管1中加入蒸馏水洗涤沉淀,静置后弃去上层清液,再加入 。 |
|
|
步骤3:
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com