
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
下列叙述不正确的是:
A. 液氯泄漏事故时,附近人员应迅速远离液氯泄漏地点,并逆风往安全区域疏散
B. 水的沸点比硫化氢高,主要原因是水分子间能形成氢键
C. 反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
D. 常温下浓硫酸可贮存于铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的是离子组是:
A. K+、Na+、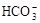 、
、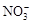
B. Na+、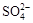 、Cl-、ClO-
、Cl-、ClO-
C. H+、Mg2+、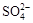 、
、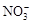
D. Ag+、K+、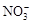 、Na+
、Na+
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
下列除去杂质的实验方法正确的是:
A. 除去CO中少量O2:通过灼热的Cu网后收集气体
B. 除去K2CO3固体中少量NaHCO3:置于坩埚中加热
C. 用过量氨水除去Al3+溶液中的少量Fe3+
D. 除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
下列关于Cl、N、S等非金属元素化合物的说法正确的是:
A.漂白粉的成分是次氯酸钙
B.实验室可用浓硫酸干燥氨气
C.实验室可用NaOH 处理Cl2 和HCl 废气
D.Al2(SO4)3 可除去碱性废水及酸性废水中的悬浮颗粒
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
目前人类已发现的非金属元素除稀有气体外,共有16种。下列对这16种非金属元素的相关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成酸:
A.只有②③正确
B.只有①③正确
C.只有④正确
D.①②③④均不正确
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是:
A.密闭容器中CuO和C高温反应的气体产物: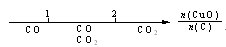
B.Fe在Cl2中的燃烧产物: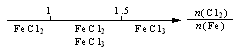
C.AlCl3溶液中滴加NaOH后铝的存在形式: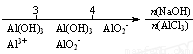
D.氨水与SO2反应后溶液中的铵盐: 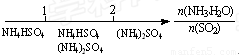
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
在pH为4-5的环境中,Cu2+和Fe2+不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸汽加热到80℃左右。在漫漫加入粗氧化铜(含杂质FeO),充分搅拌使之溶解。欲除去所得CuCl2溶液中的杂质离子,下列方法中可行的是:
A.加入HNO3将Fe2+氧化成Fe3+,再加水稀释至pH4-5
B.向溶液中通入Cl2,再加入CuO粉末调节至pH4-5
C.向溶液中通入Cl2,在通入NH3调节至pH4-
D.向溶液中通入H2O2, 再加入CuO粉末调节至pH4-5
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:选择题
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比为3∶4,D能分别与A、B、C形成电子总数相等的分子X、Y、Z。下列叙述正确的是:
A. X、Y、Z的稳定性逐渐减弱
B. A、B、C、D只能形成5种单质
C. X、Y、Z三种化合物的熔、沸点逐渐升高
D. 自然界中存在多种由A、B、C、D四种元素组成的化合物
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:实验题
(16分)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定,溶液浓度相同)。
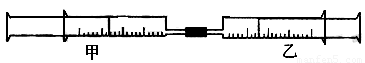
试回答下列问题:
|
实验序号 |
甲针筒内物质 |
乙针筒内物质 |
甲针筒的现象 |
|
1 |
10mLFeSO4溶液 |
10mLNH3 |
生成白色沉淀,后变色 |
|
2 |
10mLAlCl3溶液 |
40mLNaOH溶液 |
|
|
3 |
10mL紫色石蕊试液 |
25mLCl2 |
|
|
4 |
15molCl2 |
40mLNH3 |
|
⑴实验1中,沉淀最终变为 色,写出沉淀变色的化学方程式 。
⑵实验2甲针筒内的现象是: ,写出有关反应的离子方程式: 、 。
⑶实验3甲针筒内的现象是: ,反应后乙针筒内有少量的残留气体,正确的处理方法是将其通入 溶液中。
⑷实验4中,已知:3Cl2+2NH3=N2+6HCl。甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为 。
查看答案和解析>>
科目: 来源:2011-2012学年广东省高三第二次月考理科综合试题(化学部分) 题型:实验题
(16分)我国化学侯德榜(右图)改革国外的纯碱生产工艺,生产流程可简要表示如下:
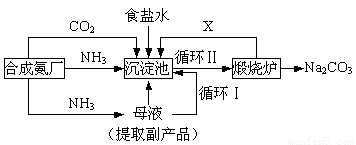

沉淀池中四种盐在不同温度下的溶解度(g / 100 g水)表
|
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
60℃ |
100℃ |
|
|
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
39.8 |
|
NH4HCO3 |
11.9 |
15.8 |
21.0 |
27.0 |
-① |
- |
- |
- |
|
NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
16.4 |
- |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.3 |
77.3 |
①>35℃NH4HCO3会有分解
请回答:
(1)沉淀池中反应温度控制在30℃~35℃,是因为若高于35℃,则 ,若低于30℃,则 ;为控制此温度范围,采取的加热方法为 。
(2) 沉淀池中发生的化学反应方程式是 。
(3)副产品的一种用途为 ,写出上述流程中X物质的分子式 。
(4)加料完毕后,继续保温30分钟,目的是 。静置后只析出NaHCO3晶体的原因是 。用蒸馏水洗涤NaHCO3晶体的目的是除去 杂质(以化学式表示)。
(5) 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com