
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
下列各组离子,一定能在指定环境中大量共存的是
A.在含有大量I-离子的溶液中:Cl¯、Fe3+、Al3+、Cu2+
B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存
C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯
D.在加入Al能放出大量H2的溶液中:NH4+、SO42¯ 、C1¯、HCO3¯
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
设NA表示阿伏加德罗常数的值,下列叙述不正确的是
A.标准状况下,11.2 L四氯化碳所含分子数为0.5NA
B.0.1molNa2O2与足量CO2反应,转移电子数为0.1NA
C.1L 1 mol·L-1的FeCl3溶液中Fe3+的数目小于NA
D.在标准状况下,11.2L氖气中含有氖原子数为0.5NA
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
下列化学实验事实及其解释都正确的是
A.在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性
B.向SO2 水溶液中滴加盐酸酸化的BaCl2 溶液,有白色沉淀生成,说明BaSO4 难溶于盐酸
C.在淀粉溶液中加入适量稀硫酸微热,再加少量新制氢氧化铜浊液加热,无红色沉淀,说明淀粉未水解
D.向2.0mL浓度均为0.1mol·L-1 的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1 AgNO3 溶液,振荡,沉淀呈黄色,说明AgCl 的Ksp比AgI 的Ksp大
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
HA为酸性略强于醋酸的一元弱酸。在0.1mol·L-1 NaA溶液中,离子浓度关系正确的是
A. c(Na+)+c(OH—)= c(A— )+c(H+)
B.c(Na+)= c(A—)+c(HA)
C. c(Na+)>c(OH—) > c(A—) > c(H+)
D.c(Na+)> c(A—)> c(H+)> c(OH—)
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
下图为一原电池的结构示意图,下列说法中,不正确的是
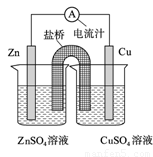
A. 原电池工作时的总反应为Zn+Cu2+=Zn2++Cu
B.原电池工作时,Zn电极流出电子,发生氧化反应
C.如将Cu电极改为Fe电极,CuSO4溶液改为FeSO4溶液,则Zn电极依然作负极
D.盐桥中装有琼脂-饱和氯化钾溶液,则盐桥中的K+移向ZnSO4溶液
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是
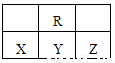
A.R的气态氢化物比Y的气态氢化物稳定
B.原子半径大小顺序是Z>Y>X
C.Y、R形成的化合物YR2能使KMnO4溶液褪色
D.X、Y、Z中X的最高价氧化物对应的水化物的酸性最强
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:选择题
下列装置或操作能达到实验目的的是
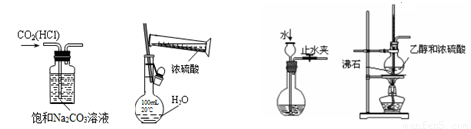
A.除去CO2中的HCl B.稀释浓硫酸 C.检查装置气密性 D.实验室制备乙烯
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:填空题
(16分)龙胆酸甲酯是制取抗心律失常药物——氟卡尼的中间体。
I、已知龙胆酸甲酯结构如图所示。

(1)龙胆酸甲酯的分子式为 ,它的含氧官能团名称为 。
(2)下列有关龙胆酸甲酯的描述,不正确的是 (填字母)。
A.不能发生消去反应 B.难溶于水
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是
。(不用写反应条件)
II、已知X及其他几种有机物存在如下转化关系,且测得转化过程中的C4H8为纯净物:

回答以下问题:
(4)写出满足下列条件的龙胆酸的一种同分异构体的结构简式
①能发生银镜反应;②能使FeCl3溶液显色;③酯类。
(5)写出B生成C的化学方程式 ,它的反应类型是
反应。
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:填空题
(16分)尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
第1步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1= —330.0 kJ·mol-1
H2NCOONH4(氨基甲酸铵) (l) △H1= —330.0 kJ·mol-1
第2步:H2NCOONH4(l) H2O(l)+H2NCONH2(l)
△H2=+226.3 kJ·mol-1
H2O(l)+H2NCONH2(l)
△H2=+226.3 kJ·mol-1
(1)写出工业合成尿素的热化学方程式:
(2)下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.添加高效催化剂 D.定时分离尿素
(3)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图所示:
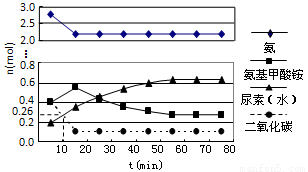
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= 。
(4)工业上合成氨常与尿素生产联合进行以提高经济效益,合成氨的热化学方程式如下:
N2(g) + 3H2(g)  2NH3(g)
△H = —92.4 kJ/mol
2NH3(g)
△H = —92.4 kJ/mol
请在答题卡的坐标图中,画出反应过程中体系的能量变化图(进行必要的标注)。
(5)有一工业投产前小实验:在一定温度和压强下,将6 molH2和2 molN2在2L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数约为11.1%(即1/9),此时H2的转化率是多少?(写出计算过程,计算结果保留3位有效数字。)
查看答案和解析>>
科目: 来源:2011-2012学年广东省南海区高三摸底考试理综化学试卷 题型:填空题
(16分)铝土矿的主要成分为Al2O3。生产铵明矾[NH4Al(SO4)2·12H2O]和Z(其水溶液可用于伤口消毒)的工艺流程图如下:
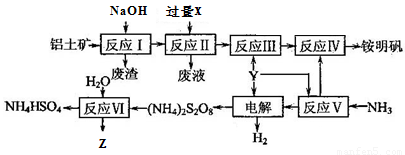
(1)反应Ⅰ的主要离子方程式是__________________________ 。
(2)已知反应Ⅱ中会生成氢氧化铝沉淀,则加入过量的X为_________(填化学式)。
(3)“电解”时,用惰性材料作电极,则阴极反应可表示为 _________ 。
(4)流程中可以循环使用的物质是 。
(5)反应Ⅵ的化学方程式为 __________ ,其中的还原剂是____________。
(6)已知铵明矾的许多用途和明矾类似,请说明铵明矾的净水原理_________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com