
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
已知反应:2 E (l)  U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。
U (l) 。取等量的E,分别在20℃、50℃测得E的转化率随时间变化的关系曲线(Y-t)如右图所示。
则下列说法正确的是
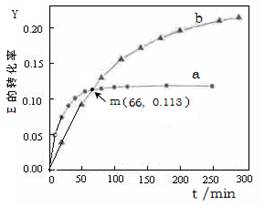
A.该反应的∆H > 0
B.b代表50℃下E的Y-t曲线
C.m点(66,0.113)时有: ∆n (E,20℃) = ∆n (E,50℃)
D.升高温度可以缩短达到平衡的时间,提高E的转化率
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
能正确表示下列反应的离子方程式是
A.碳酸氢钠溶液中加入少量氢氧化钡:HCO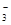 +
Ba2+ + OH- == BaCO3↓+ H2O
+
Ba2+ + OH- == BaCO3↓+ H2O
B.大理石跟稀盐酸反应:CaCO3 + 2H+ == Ca2+ + H2O + CO2↑
C.氢氧化镁跟稀硫酸反应:OH-+ H+ == H2O
D.碳酸氢铵溶液中加入足量氢氧化钠溶液:NH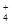 +
OH- == NH3·H2O
+
OH- == NH3·H2O
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
常温下用0.10 mol /L KOH溶液,滴定0.10 mol /L CH3COOH溶液,有关滴定过程中的说法正确的是
A.滴定终点时:溶液的pH=7
B.滴定终点时:c(K+) = c(CH3COO-),c(H+) < c(OH-)
C.当溶液pH=7时:c(K+) = c(CH3COO-) + c(CH3COOH)
D.接近滴定终点时:c(K+) + c(H+) = c(CH3COO-) + c(OH-)
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
下列实验过程中始终没有明显现象的是
A.往AlCl3溶液中逐滴加入NaOH溶液
B.往Fe(NO3)2溶液中逐滴加入稀H2SO4
C.CO2通入饱和Na2CO3溶液中
D.往Ba(OH)2溶液中逐滴加入稀HCl溶液
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
Na2FeO4是一种新型水处理剂,可以通过下列反应制取:
□NaClO + □Fe2(SO4)3 + □ M == □Na2FeO4 + □NaCl + □H2O + □ N
下列有关该反应的说法错误的是
A.Na2FeO4是氧化产物,有强氧化性,可消毒杀菌,其还原产物能吸附水中杂质
B.氧化剂与还原剂的物质的量之比为3∶1
C.M与N分别是NaOH和H2SO4
D.若有3 mol NaClO完全反应,则生成2 mol Na2FeO4
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:选择题
在含0.075 mol KHCO3的溶液中,加入0.025 mol KOH,然后向溶液中滴加1.0 mol /L稀盐酸。下列图像能正确表示加入盐酸体积与生成CO2的物质的量的关系的是
|
|
|
|
|
|
A |
B |
C |
D |
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:填空题
(14分)X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
原子最外层电子数是次外层的三倍 |
|
Z |
单质及其化合物的焰色反应为黄色 |
|
W |
W元素基态原子的M层全充满,N层只有一个电子 |
⑴ X位于元素周期表第 族。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于 晶体。
⑵ X与Y中电负性较强的是(填元素符号) ;XY2的电子式是 ,分子中存在 个σ键。
⑶Z2Y2中含有的化学键类型有 。阴、阳离子的个数比为 。
⑷W的基态原子核外电子排布式是 。
⑸废旧印刷电路板上有W的单质A。用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A。已知:
A(s)+H2SO4 (aq) == ASO4(aq) + H2(g) ΔH=+64.4kJ·mol-1
2H2O2(l) == 2H2O(l) + O2(g) ΔH= -196.4kJ·mol-1
H2(g)+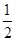 O2(g) == H2O(l) ΔH= -285.8kJ·mol-1
O2(g) == H2O(l) ΔH= -285.8kJ·mol-1
请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):
。
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:填空题
(15分)阿司匹林(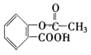 )具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药。
)具有解热、镇痛、抗炎、抗风湿和抗血小板聚集等多方面的药理作用,是应用最早、最广和最普通的解热镇痛药。
⑴阿司匹林的分子式是 ,含氧官能团的名称是 、 。
⑵写出阿司匹林跟足量NaOH溶液反应的化学方程式:
⑶水杨酸的分子式是C7H6O3,跟乙酸酐( )在催化剂作用下生成阿司匹林。则水杨酸的结构简式是
,该制取反应的反应类型是 。
)在催化剂作用下生成阿司匹林。则水杨酸的结构简式是
,该制取反应的反应类型是 。
⑷同时符合下列条件的水杨酸的同分异构体有 种。
①分子中有苯环;②能跟银氨溶液反应生成银镜;③苯环上的一硝基取代物有2种。
写出其中任一种的结构简式 。
⑸一种缓释阿司匹林的结构式如下:
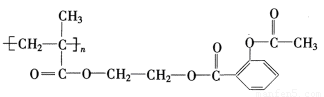
该物质在酸性条件下水解生成阿司匹林、乙二醇和一种聚合物。这种聚合物的单体的结构简式是 。
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:填空题
(14分)下图是各种不同密度的硝酸与铁反应(相同温度)时主要还原产物的分布图。请认真读图分析,回答有关问题。

⑴下列叙述中正确的是(填序号) 。
A.图中横坐标是硝酸的密度,硝酸的密度越大,其浓度越大。
B.当还原剂和温度相同时,不同浓度的硝酸被还原的产物不是单一的,只是在某浓度时,以某种产物为主而已。
C.硝酸的浓度越大,还原产物中N元素低化合价产物越多。
D.当硝酸密度大于1.3 g·cm-3时,还原产物主要为NO、NO2
⑵ 当硝酸溶液的密度为1.36 g·cm-3时,下列化学方程式中,能较准确表达Fe与过量硝酸反应的是(填序号) 。
A.2Fe + 10HNO3 == 2Fe(NO3)3 + NO↑+3NO2↑+5H2O
B.4Fe + 18HNO3 == 4Fe(NO3)3 + 3NO↑+3NO2↑+9H2O
C.3Fe + 12HNO3 == 2Fe(NO3)3 + Fe(NO3)2 + 2NO↑+2NO2↑+3H2O
⑶ 密度为1.26 g·cm-3,质量分数为50.0 %的硝酸,其物质的量浓度是 mol·L-1。
⑷ 限用下列仪器、药品验证由铁和过量1.36 g·cm-3硝酸反应产生的气体中含有NO(不考虑N2O4)。设计一个合理而简单的实验方案(仪器可选择使用,N2的用量可自由控制,加热装置和固定装置省略)。

第1步:反应并收集生成的气体:
①实验中气体发生装置应选择 (填装置序号),理由是 。
②装置的连接顺序是(填各装置接口的序号):[ ]→[ ] [ ]→[8] [9]→[ ]。
③检查装置气密性后,开始反应。待E中充满红棕色气体,停止实验。
第2步:验证E中有NO。
④ 取下试管E,倒立在F中,轻轻摇动试管。
确认生成的气体中有NO的现象是 。
查看答案和解析>>
科目: 来源:2011-2012学年安徽省黄山市高三七校联考化学试卷 题型:填空题
(15分)水是生命之源。饮用水消毒剂作为控制水质的一个重要环节,令世人关注。
⑴液氯消毒是最早的饮用水消毒方法。氯气溶于水能杀菌消毒的原因是:
。近年来科学家提出,氯气能与水中的有机物发生反应,生成的有机氯化物可能对人体有害。
臭氧(O3)是优良的水消毒剂。但当水中含溴离子(Br-)时,臭氧可氧化溴离子(Br-)为溴酸盐 (BrO- 3)。而溴酸盐 (BrO- 3)是对人体有致癌作用的化合物,我国规定饮用水中BrO- 3含量在10μg / L以下。测定BrO- 3浓度可用离子色谱法。
⑵水中的氯离子(Cl-)对BrO-3测定干扰很大,需要先除去氯离子(Cl-)。用右图的装置可除去水中的氯离子(Cl-)。
装置中Ag是 极(填电极名称),
Ag电极的电极反应式是 。

⑶ O3氧化溴离子的原理如下:

已知HBrO是一种弱酸,O3与HBrO反应很慢,BrO- 3主要是由BrO-与O3反应生成。
对影响生成BrO- 3速率的因素提出如下假设:(请你完成假设②和假设③)
假设①:反应的温度。
假设②:
假设③:
⑷设计实验验证假设①。
验证实验操作:
a. 配制250 mL 50 mg / L KBr溶液,加入 15 mL 某种pH=7的缓冲溶液(维持溶液的pH基本不变),并将溶液分为2份。
b.
实验中要测定的量是
实验结论是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com