
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:选择题
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(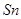 ),发生反应:
),发生反应: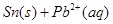

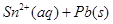 ,体系中c(Pb2+)和c(Sn2)变化关系如右图所示。下列判断正确的是
,体系中c(Pb2+)和c(Sn2)变化关系如右图所示。下列判断正确的是
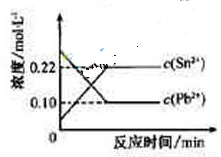
A. 往平衡体系中加入少量金属铅后,c(Pb2+)增大
B. 往平衡体系中加入少量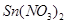 固体后,c(Sn2)变小
固体后,c(Sn2)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应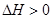
D. 25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:填空题
I.磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是 。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500°C生成白磷,反应为:
2Ca3(PO4)2+6SiO2==6CaSiO3+P4O10 10C+P4O10==P4+10CO
每生成 1molP4 时,就有 mol电子发生转移。
(3)硫代硫酸钠(Na2S2O2)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素 完全氧化,剩余的I2 用Na2S2O2溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入amolL-1I2溶液V1ml,充分反应后,用Na2S2O2溶液滴定剩余的I2,消耗bmolL-1 Na2S2O2溶液V2ml.该溶液中维生素C的物质量是 mol。
(4)在酸性溶液中,碘酸钠(KIO3)和亚硫酸钠可发生如下反映:
2IO3-+5SO32-+2H+==I2+5SO42++H2O
生成的碘可以用淀粉液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
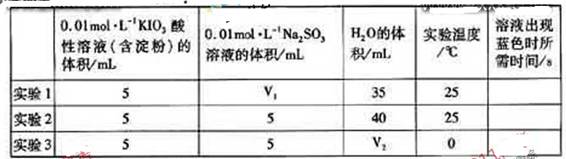
该实验的目的是______;表中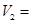 ______ML。
______ML。
II 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)钵(Ce)是地壳中含量最高的稀土元素,在加热条件下CeCl3易发生水解,无水CeCl3,可用加热CeCl3• 6H2O和NH4Cl固体混合物的方法来制备。其中,NH4Cl的作用是___________。
(6)在某强酸性混合稀土溶液中加入H2O2,调节pH ≈3. Ce5+通过下列反应形成Ce
(OH)4沉淀得以分离。完成反应的离子方程式:
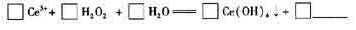
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:填空题
四氧化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成为是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
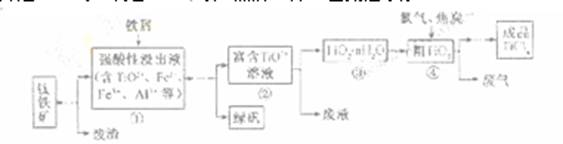
回答下列问题
( 1 ) 往①中缴入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
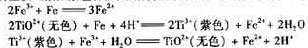
加入铁屑的作用是 。
(2)在②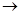 ③工艺过程中需要控制条件以形成
③工艺过程中需要控制条件以形成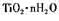 溶液,该溶液的分散质颗粒直径大大小在
范围。
溶液,该溶液的分散质颗粒直径大大小在
范围。
(3)若把③中制得得固体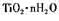 用酸清洗除去其中的
用酸清洗除去其中的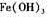 杂质,还可以制得钛白粉。已知25°C时,
杂质,还可以制得钛白粉。已知25°C时, 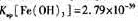 该温度下反应
该温度下反应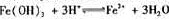 的平衡常数K= 。
的平衡常数K= 。
(4)已知:
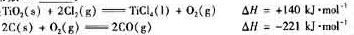
写出④中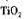 和焦炭、氧气反应生成也太
和焦炭、氧气反应生成也太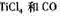 气体的热化学方程式:
气体的热化学方程式:
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项 )。
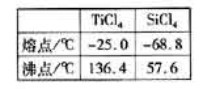
(6)依据右表信息,要精制含少量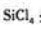 杂质的
杂质的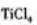 的,
的,
可采用 方法。
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:实验题
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。
Ⅰ.摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水充足搅拌、过滤。
(1)往滤渣中加入过量 NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是 。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察的现象是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO 沉淀质量,以确定碳酸钙的质量分数。
沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:________
(4)C中反应生成BcCO2的化学方程式是__________________。
(5)下列各项措施中,不能提高测定准确度的是_________(填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO2平均质量为3.94 g。则样品中碳酸钙的质量分数为__________。
(7)有人认为不必测定C中生成的 质量,只要测定装置C在吸收
质量,只要测定装置C在吸收 前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______.
前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______.
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:填空题
氮元素可以形成多种化合物。
回答以下问题:
(1)基态氮原子的价电子排布式是__________________。
(2)C、N、O三种元素第一电离能从大到小的顺许昌是_________________。
(3)肼(N2H4)分子可视为NH3 分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮化物。
①NH3 分子的空间构型是____________;N2H4分子中氮原子轨道的杂化类型是____________________。
②肼可用作火箭燃料,燃烧时发生的反应是:
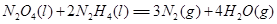
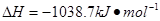
若该反应中有4mol N—H键断裂,则形成的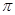 键有___________mol。
键有___________mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在________(填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体得4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物是别的是________________(填标号)。
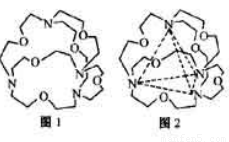
a.CF4 b. CH4 c. NH4+ d.H2O
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(福建) 题型:填空题
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶。制备它的一种配方中含有下列四种物质:
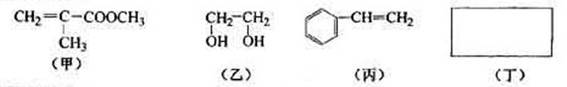
填写下列空白:
(1)甲中不含氧原子的官能团是____________;下列试剂能与甲反应而褪色的是s___________(填标号)
(2)甲的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式:_______
(3)淀粉通过下列转化可以得到乙(其中A-D均为有机物):
 A的分子式是___________,试剂X可以是___________。
A的分子式是___________,试剂X可以是___________。
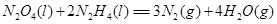
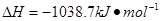
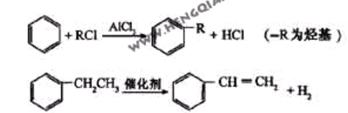
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是 。
(5)化合物丁仅含碳、氢、氧三种元素,相对分子质量为110.丁与FeCl3溶液作用显现特征颜色,且丁分子中烃基上的一氯取代物只有一种。则丁的结构简式为 。
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(重庆) 题型:选择题
一定量的Fe与过量的稀硫酸反应制取氢气,一定温度下为加快反应速率而又不影响氢气的量,可向其中加入少量
A.K2SO4固体 B.Zn 粉 C.SO3 固体 D.CuSO4 晶体
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(重庆) 题型:选择题
下列条件一定能使反应速率增大的是
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物 ⑤加入MnO2
A.② B.②③ C.①②⑤ D.全部
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(重庆) 题型:选择题
用于净化汽车尾气的反应:2NO(g)+2CO(g) 2CO2(g)+N2(g),已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是
2CO2(g)+N2(g),已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是
A.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
B.提高尾气净化效率的常用方法是升高温度
C.提高尾气净化效率的最佳途径是研制高效催化剂
D.570 K时该反应正向进行的程度很大,故使用催化剂并无实际意义
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(重庆) 题型:选择题
反应H2(g)+I2(g)  2HI(g)的平衡常数为K1;反应HI(g)
2HI(g)的平衡常数为K1;反应HI(g) 1/2H2(g)+1/2I2(g)的平衡常数为K2,则K1、K2的关系为(平衡常数为同温度下的测定值)
1/2H2(g)+1/2I2(g)的平衡常数为K2,则K1、K2的关系为(平衡常数为同温度下的测定值)
A.K1=2K2 B. K1=1/K22 C.K1=K22 D.K1=1/2K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com