
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(全国) 题型:实验题
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:
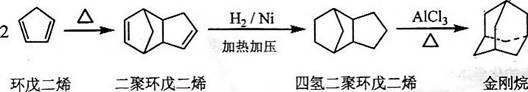
请回答下列问题:
(1)环戊二烯分子中最多有_____________个原子共平面:
(2)金刚烷的分子式为___________,其分子中的CH2:基团有______个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
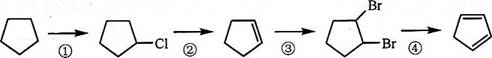
其中,反应①的产物名称是__________,反应②的反应试剂和反应条件
是__________,反应③的反应类型是__________;
(4)已知烯烃能发生如下反应:
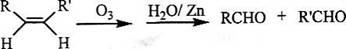
请写出下列反应产物的结构简式:

(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(-CH3,-CH2R,-CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构):
___________________________________________________________________________
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
下列说法不正确的是
A.麦芽糖及其水解产物均能发生银镜反应
B.用溴水即可鉴别苯酚溶液,2,4-已二烯和甲苯
C.在酸性条件下,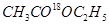 的水解产物是
的水解产物是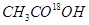 和
和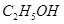
D.用甘氨酸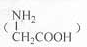 和丙氨酸
和丙氨酸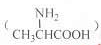 缩合最多可形成4种二肽
缩合最多可形成4种二肽
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
结合右图判断,下列叙述正确的是

A.Ⅰ和Ⅱ种正极均被保护
B. Ⅰ和Ⅱ中负极反应均是
C. Ⅰ和Ⅱ中正极反应均是
D. Ⅰ和Ⅱ中分别加入少量 溶液,均有蓝色沉淀
溶液,均有蓝色沉淀
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
下列与处理方法对应的反应方程式不正确的是
A.用NaS去除废水中的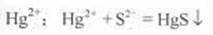
B.用催化法处理汽车尾气中的CO和NO:
C.向污水中投放明矾,生成能凝聚悬浮物的胶体:
D.用高温催化氧化法去除烃类废气
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
25℃、101kPa 下:

下列说法正确的是
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa 下,Na2O2(s)+2 Na(s)= 2Na2O(s) 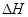 =-317kJ/mol
=-317kJ/mol
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
下列实验方案中,不能测定Na2CO3和NaCHO3,混合物中Na2CO3质量分数的是
A.取a克混合物充分加热,建中b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得h克固体。
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:选择题
已知反应:2CH3COCH3(l)  CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0 ℃和20 ℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
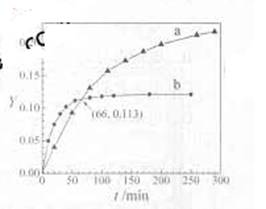
A. b代表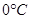 下CH3COCH3的Y-t曲线
下CH3COCH3的Y-t曲线
B. 反应进行到20min末,H3COCH3的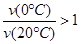
C. 升高温度可缩短反应达平衡的时间并能提高平衡转化率
D. 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的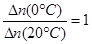
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:填空题
在温度t1和t2下,X2(g)和 H2反应生成HX的平衡常数如下表:
|
化学方程式 |
K (t1 ) |
K (t2) |
|
|
1.8 |
|
|
|
|
|
|
|
|
|
|
|
43 |
34 |
(1)已知t2 〉t1,HX的生成反应是 反应(填“吸热”或“放热”)。
(2)HX的电子式是 。
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是 。
(4)X2都能与H2反应生成HX,用原子结构解释原因: 。
(5)K的变化体现出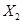 化学性质的递变性,用原子结构解释原因:__________,原子半径逐渐增大,得电子能力逐渐减弱。
化学性质的递变性,用原子结构解释原因:__________,原子半径逐渐增大,得电子能力逐渐减弱。
(6)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_______(选填字母)
a. 在相同条件下,平衡于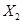 的转化率逐渐降低
的转化率逐渐降低
b. 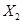 与
与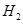 反应的剧烈程度逐渐减弱
反应的剧烈程度逐渐减弱
c. HX的还原性逐渐
d. HX的稳定性逐渐减弱
查看答案和解析>>
科目: 来源:2011年普通高等学校招生全国统一考试化学卷(北京) 题型:填空题
氯碱工业中电解饱和食盐水的原理示意图如右图所示
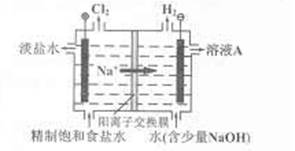
(1)溶液A的溶质是 ;
(2)电解饱和食盐水的离子方程式是
(3)电解时用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用
(4)电解所用的盐水需精制。去除有影响的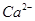 、
、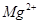 ,NH+3,
,NH+3,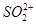 ,[
,[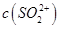 >
>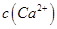 ]。
]。
精致流程如下(淡盐水和溶液A来电解池):

①盐泥a除泥沙外,还含有的物质是 。
②过程Ⅰ中将NH4+转化为N2的离子方程式是
③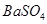 的溶解度比
的溶解度比 的小,过程Ⅱ中除去的离子有
的小,过程Ⅱ中除去的离子有
④经过程Ⅲ处理,要求盐水中c 中剩余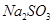 的含量小于5mg /l ,若盐水b中
的含量小于5mg /l ,若盐水b中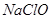 的含量是7.45 mg /l ,则处理10m3 盐水b ,至多添加10%
的含量是7.45 mg /l ,则处理10m3 盐水b ,至多添加10% 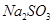 溶液 kg(溶液体积变化忽略不计)。
溶液 kg(溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com