
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
有Fe2++H++NO3-→Fe3++NH4++H2O这样一个变化过程,下列叙述不正确的是
A.氧化剂和还原剂的物质的量之比为1:8
B.该过程说明Fe(NO3)2溶液不宜加酸酸化
C.每1 mol NO3-发生氧化反应,转移8 mol 电子
D.若把该反应设计为原电池,则负极反应为Fe2+- e- = Fe3+
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
X、Y、Z、R均为短周期元素,X、Y、R同周期,其中R的质子数最大;X、Z同主族。 X的原子结构示意图为: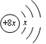 ,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7。下列叙述正确的是
,Y的原子半径在短周期中最大,Y与R最外层电子数之比为1:7。下列叙述正确的是
A.离子半径:X>Z>Y B.对应气态氢化物的稳定性:R>X>Z
C.对应氢化物的沸点:R>Z>X D.Z与X、Y与R形成化合物的晶体类型相同
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
下列溶液中各微粒的浓度关系正确的是
A.等pH值的氨水、KOH溶液、Ba(OH)2溶液中: c(NH4+)=c(K+)=2c(Ba2+)
B.0.1 mol/L 的CH3COONa溶液中:c(CH3COO-) > c(Na+) >c(OH-) >c(H+)
C.常温时向NH4HSO4溶液中滴加NaOH溶液至pH=7:c(NH4+)+c(Na+)= c(SO42-)
D.将10 mL 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中:
c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
绿原酸是咖啡的热水提取液的成分之一,绿原酸结构简式如图,下列关于绿原酸判断不正确的是
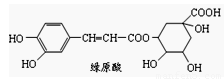
A.绿原酸既可以催化加氢,又可以使酸性KMnO4溶液褪色
B.绿原酸的官能团中有羧基
C.1mol绿原酸与足量NaOH溶液反应,最多消耗2mol NaOH
D.绿原酸可以与FeCl3溶液发生显色反应
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:选择题
某固体混合物可能含有下列物质Na2O2、Na2CO3、NaHCO3、NaCl,向混合物中加入足量的盐酸,有气体放出,将放出的气体通入足量的NaOH溶液后,气体体积减少了一部分,若将上述混合物在空气中充分加热,也有气体放出,下列判断正确的是
A.混合物中一定含有Na2O2、NaHCO3 B.混合物中一定不含有Na2CO3和NaCl
C.混合物一定不含有Na2O2和NaCl D.混合物中一定含有Na2O2、Na2CO3、NaHCO3
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:填空题
A、B、C三种强电解质,它们在水中电离出的离子为Na+ 、Ag+ 、NO3- 、SO42- 、 Cl-,在如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了10.8克。常温下各烧杯中溶液的pH与电解时间t的关系如图所示。据此回答下列问题:
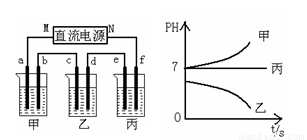
(1)M为电源的_______极(填写“正”或“负”),甲、乙两个烧杯中的电解质分别为_______、_______(填写化学式)。
(2)计算电极f上生成的气体为_______mol。
(3)写出乙烧杯中的电解反应方程式: _______________________________________。
(4)若电解后甲溶液的体积为10L,则该溶液的pH为___________ 。
(5)要使丙恢复到原来的状态,应加入适量的 (填写化学式)。
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:填空题
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应①②是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化.

(1)化合物A中含有的短周期元素是 (写元素符号),E的化学式_______。
(2)如何检验化合物N中的阳离子 。
(3)写出J与F反应的离子方程式: ,G与H反应的化学方程式: 。
(4)等物质的量F和H的混合气体通入品红溶液中的现象为 ,原因是(用化学反应方程式表示) 。
(5)已知C与D反应生成1.7g G 时放出4.26kJ的热量,则该反应的热化学方程式为
。
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:实验题
二氧化锰(MnO2)与浓盐酸混合加热可得到氯气、氯化锰等,下图是制取并探究Cl2化学性质的装置图。
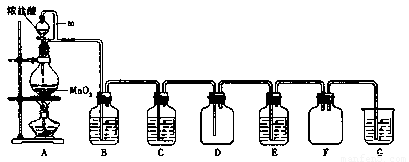
(1)写出圆底烧瓶中反应的化学方程式 。
(2)A中m管的作用是 ;装置F的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是 ,C中应盛放的试剂是 。
(4)E中若装有FeCl2溶液,反应的离子方程式为 ;E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,化学小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通人HCl气体,加热
b.稀盐酸滴人MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是 ;实验c的目的是 。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三上学期第四次月考(理综)化学部分 题型:实验题
有机物A是重要的合成原料,在医药、染料、香料等行业有着广泛的应用。由A可以制得麻黄碱和其他很多物质。现有如下转化关系图(略去了由A→G,G→麻黄碱的部分反应物和条件):
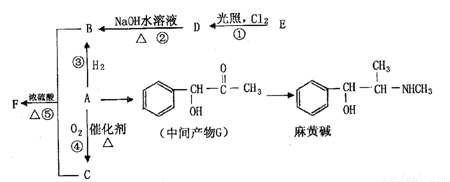
请回答下列问题:
(1)关于麻黄碱下列说法正确的是 (填字母)。
a.麻黄碱的分子式为C10H15NO
b.1mol麻黄碱可以对应消耗1molHCl或NaOH
c.麻黄碱可以发生消去和酯化反应
d.麻黄碱属于芳香烃
(2)已知有机物A的相对分子质量为106,A中含碳、氢、氧的质量之比为42:3:8,
则A的含氧官能团名称是 ;检验该官能团的实验是 。
(3)反应①~⑤中属于取代反应的是 (填序号)。
(4)写出D—B的化学方程式 。
(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式 。
(6)写出符合下列条件的同分异构体的结构简式 。
①与中间产物G互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
|
|
溶解性 |
沸点 |
|
A |
微溶于水 |
179.0℃ |
|
E |
不溶于水 |
110.8℃ |
A可以由E制取,制取工艺中得到的是A、E混合物,分离该混合物的方法是 。
查看答案和解析>>
科目: 来源:2010-2011学年贵州省高三第四次月考(理科综合)化学部分 题型:选择题
化学与社会、生活密切相关,下列有关说法不正确的是
A.利用清洁能源代替化石燃料,有利于节约资源、保护环境
B.食品添加剂种类很多,其中一种为苯甲酸钠,它是苯的一种同系物所对应的钠盐
C.生铁在潮湿的空气中易生锈的原因是发生了电化学腐蚀
D.乙醇属于可再生能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com