
科目: 来源:不详 题型:单选题
| A.H2S+2HNO3═S↓+2NO2↑+2H2O |
| B.CuO+2HNO3═Cu(NO3)2+H2O |
| C.4HNO3═4NO2↑+O2↑+2H2O |
| D.3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.制高铁酸钾用ClO-做还原剂 |
| B.制备高铁酸钾时1molFe(OH)3得到3mol电子 |
| C.高铁酸钾中铁的化合价为+6,其氧化性强于ClO-的氧化性 |
| D.用高铁酸钾处理水时,利用了其强氧化性,且其还原产物能水解产生具有强吸附能力的胶体 |
查看答案和解析>>
科目: 来源:南京二模 题型:单选题
| ||
| A.该反应中,Al2O3是氧化剂 |
| B.该反应中,N2是还原剂 |
| C.该反应中,C是还原剂 |
| D.该反应中每生成2molAlN,N2得到3mole- |
查看答案和解析>>
科目: 来源:不详 题型:问答题
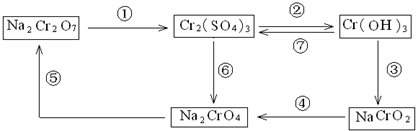
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应①不是氧化还原反应 |
| B.该生产过程不产生任何污染 |
| C.反应①中,每有5.6gFe参加反应转移0.8mol电子 |
| D.反应②中的z、m、k依次是5、3、7 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| A.Y是SO42- |
| B.a=8 |
| C.Cr2O72-被氧化成Cr3+ |
| D.生成1molCr3+时转移的电子数是3×6.02×1023 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.H2O2在上述3个反应中均做氧化剂 |
| B.H2O2氧化性强于HIO,还原性弱于I2 |
| C.上述过程中每生成1mol氧气,消耗1mol双氧水 |
| D.在反应后的溶液中加入淀粉,溶液呈现蓝色 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
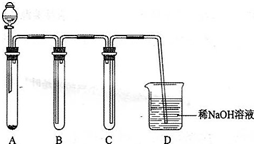
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.石墨烯是一种高分子材料 |
| B.甲醇是一种含极性键的非极性分子 |
| C.18O2和16O2互称为同位素 |
| D.由N5变成N2是化学变化,属于非氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com