
科目: 来源:2010-2011学年浙江省杭州市高三市二测模考(理综)化学部分 题型:填空题
已知a、e、I为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
|
粒子代码 |
a |
e |
I |
|
原子核数 |
单核 |
两核 |
四核 |
|
粒子的电荷数[来源:学,科,网Z,X,X,K] |
一个单位正电荷 |
一个单位负电荷 |
0 |
物质A由a、e 构成, B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①—⑤ 都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去。
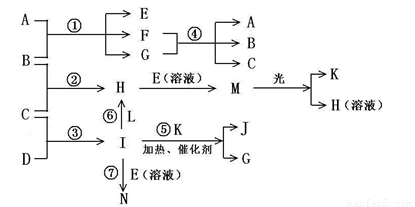
请填写下列空白:
(1)写出下列物质的化学式:B__________,J__________。
(2)写出下列反应的离子反应方程式:
H + E(溶液)→M____________________________________________________,
F + G →A + B + C________________________________________;
(3)E(溶液)能与I以1∶2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出N的结构式__________;
(4)L是由3种元素构成的分子,能与I以1∶2的物质的量之比反应生成尿素CO(NH2) 2 和物质H,写出L的电子式__________;
(5)反应③用于工业生产它应在_______________进行(填设备名称);反应④用于工业生产时为了防止B和C混合反应产生危险,所使用的一种特殊材料的名称为__________,在该工业生产中它具有的特殊的性质是________________________。
(6)常温下,实验室模拟工业反应④的过程如下图所示,标况下,当电极上产生112mL(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=__________。(假设气体完全逸出,溶液体积不变)
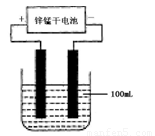
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三市二测模考(理综)化学部分 题型:填空题
已知25℃时部分弱电解质的电离平衡常数数据如下表:
|
化学式 |
CH3COOH |
H2CO3 |
HClO |
|
|
平衡常数 |
Ka=1.8×10-5 |
Ka1=4.3×10-7 |
Ka2=5.6×10-11 |
Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液:a.CH3COOH b.Na2CO3 c.NaClO d.NaHCO3; PH由小到大的排列顺序是___________________________
(2)常温下,0.1mol·L-1的的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是____
A.c(H+) B.c(H+)/ c(CH3COOH) C. c(H+)·c(OH-) D. c(OH-)/ c(H+)
E. c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100mlPH=2的CH3COOH与一元酸HX,加水稀释过程中PH与溶液体积的关系如图所示,则HX的电离平衡常数_________CH3COOH的电离平衡常数(填大于小于或等于)理由是______________________
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得PH=6,则溶液中C(CH3COO-)—c(Na+)=____________mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=__________

查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三市二测模考(理综)化学部分 题型:填空题
某氯化铁与氯化亚铁的混合物。现要测定其中铁元素的质量分数,实验按以下步骤进行:
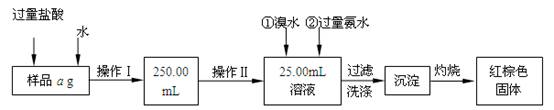
Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒外,还必须有 、 ,(填仪器名称)
(2)请写出加入溴水发生的离子反应方程式 ,
(3)将沉淀物加热,冷却至室温,用天平称量其质量为b1 g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3g,则接下来还应进行的操作是
。
若蒸发皿质量是W1 g,蒸发皿与加热后固体总质量是W2 g,则样品中铁元素的质量分数是
Ⅱ.有同学提出,还可以采用以下方法来测定:

(1)溶解样品改用了硫酸,而不用盐酸,为什么
(2)选择的还原剂是否能用铁 (填“是”或“否”),原因是:
(3)若滴定用掉c mol/L KMnO4溶液bmL,则样品中铁元素的质量分数是
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三市二测模考(理综)化学部分 题型:填空题
28.(15分)下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
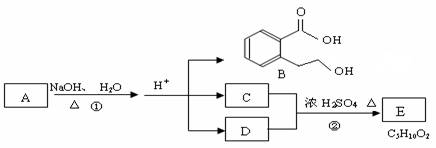
根据上图回答问题:
(1)C分子中的官能团名称是 ______________;化合物B不能发生的反应是 (填字母序号):
a 加成反应 b取代反应 c消去反应 d酯化反应 e水解反应 f 置换反应
(2)反应②的化学方程式是___________ _。
(3)试分析反应②加热的原因。
Ⅰ、 。;
Ⅱ、 。。
(4)A的结构简式是 __________________ 。
(5)同时符合下列三个条件的B的同分异构体的数目有 个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3 溶液发生显色反应。
写出其中任意一个同分异构体的结构简式 。
(6)常温下,将C溶液和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
C物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
|
m |
0.1 |
0.1 |
pH=9 |
|
n |
0.2 |
0.1 |
pH<7 |
从m组情况分析,所得混合溶液中由水电离出的c(OH-)= mol·L-1。
n组混合溶液中离子浓度由大到小的顺序是 ___________。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
下列说法正确的是
A.2010年诺贝尔化学奖授予“钯催化交叉偶联反应”的研究,采用钯催化可将碳原子连接在一起制造新的有机材料,所以钯催化剂能催化所有类型的有机反应。
B.把CO中毒的病人放入高压氧仓中解毒,其原理符合勒夏特列原理
C.日常生活中无水乙醇常用于杀菌消毒
D.“绿色荧光蛋白质”是不可降解的高分子化合物,其水溶液有丁达尔效应
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
NA表示阿伏加德罗常数值。下列说法正确的是
A.1mol Na2O2与足量CO2充分反应转移的电子数为2NA
B.标准状况下,2.24 L CHCl3的分子数为0.1 NA
C.t℃时,1L pH=6的纯水中,含1×10-6 NA个OH-
D.向FeI2溶液中通入适量氯气,当有1mol Fe2+被氧化时,总共转移电子的数目为1 NA
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
下列装置所示的实验中,能达到实验目的的是
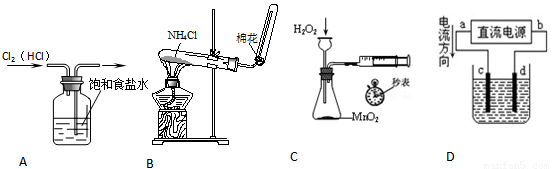
A.除去Cl2中的HCl杂质
B.实验室制取NH3
C.定量测定H2O2分解化学反应速率
D.c为粗铜,d为纯铜,溶液为硫酸铜溶液,电解精炼铜
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
赫克反应、根岸反应和铃木反应已成为化学家们制造复杂化学分子的“精致工具”,在科研、医药和电子等领域已经广泛应用。下例是由铃木反应合成出来的一种联苯的衍生物:
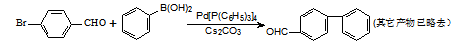
下列叙述正确的是
A.1 mol该联苯的衍生物在一定条件下最多可和7 mol H2发生加成反应
B.该联苯的衍生物属于芳香烃
C.该联苯的衍生物苯环上的一硝基取代产物有7种
D.该反应为加成反应,且原子利用率达100%
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学设计了实验方案(见下表),将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
|
实验 试剂 |
甲 |
乙 |
丙 |
丁 |
|
4 mol·L-1H2SO4/mL |
20 |
V1 |
V2 |
V3 |
|
饱和CuSO4溶液/mL |
0 |
2.5 |
V4 |
10 |
|
H2O/mL |
V5 |
V6 |
8 |
0 |
|
收集气体所需时间/s |
t1 |
t2 |
t3 |
t4 |
下列说法正确的是
A.t1 < t2 < t3 < t4 B.V4=V5=10
C.V6=7.5 D.V1<V2<V3<20
查看答案和解析>>
科目: 来源:2010-2011学年浙江省杭州市高三第二次质检(理综)化学部分 题型:选择题
下列化学方程式或离子方程式中,正确的是
A.用浓硫酸与4-溴-1-丁醇加热发生消去反应:
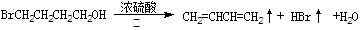
B.水杨酸(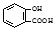 )中加入NaHCO3溶液:
)中加入NaHCO3溶液: +2HCO3-→
+2HCO3-→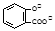 +2CO2↑+2H2O
+2CO2↑+2H2O
C. 向CuSO4溶液中滴加过量的氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2NH4+
D.用侯氏制碱法制得NaHCO3 : Na++NH3+CO2+H2O = NaHCO3↓+NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com