
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:选择题
下列关于有机化合物1和2的说法中正确的是

A.有机物1和2互为同分异构体
B.有机物1和2在氢氧化钠的乙醇溶液中均可发生消去反应
C.有机物1和2中所有原子均共平面
D.有机物2能使酸性高锰酸钾溶液褪色,而1不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:选择题
下列叙述正确的是
A.H2热值为142.9 kJ·g-1,则氢气燃烧的热化学方程式可表示为:
2H2(g)+ O2(g)= 2H2O(l) △H=-285.8kJ·mol-1
B.Al3+、Cu2+、SO42-、F-能在溶液中大量共存
C.硫酸亚铁溶液在空气中发生氧化反应:4 Fe2++ O2+4H+= 4 Fe3++2H2O
D.已知KSP(Ag2SO4)= 1.4×10—5,则向100mL0.01mol·L—1的Na2SO4溶液中加入
1 mL0.01mol·L—1的AgNO3溶液,有白色沉淀生成
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:选择题
某混合溶液中可能含有下列离子中的若干种:K+、Na+、Fe2+、Fe3+、SO42-、NO2—、CO32-,现取三份20mL该溶液进行如下实验:
(1)第一份加入足量盐酸,无任何气体产生
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧,最后得到xg固体
(3)第三份滴加0.10 mol·L—1酸性KMnO4溶液,消耗其体积为VmL
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色
根据上述实验,以下说法正确的是
A.原混合溶液中只存在Na+、Fe3+、SO42—,不可能存在K+、CO32—
B.由实验(1)无法推断原混合溶液中是否含有SO42—
C.由实验(2)、(3)可判定原混合溶液中是否含有Fe3+
D.由实验(3)可判定原混合溶液中存在NO2—
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:填空题
甲、乙、丙是分别由H、C、O、Si、Al、Cu等六种元素中的两种或多种元素组成的化合物。已知甲、乙、丙均不含结晶水,含化合物甲的矿物是工业上电解法冶炼某种常见金属单质的原料,经检测甲是一种高熔点化合物,能溶于强酸、强碱溶液;化合物乙是光导纤维的主要成分;化合物丙为一种呈深蓝色的碱式盐,将34.6g丙隔绝空气加热分解生成24g黑色固体X、无色酸性气体Y(标准状况下,密度为1.96 g/L)和水。生成的Y折合成标准状况下的体积为4.48L。固体X难溶于水,能溶于硫酸,形成蓝色溶液。请回答下列问题:
(1)写出气体Y的结构式 ▲ ,化合物丙的化学式 ▲ 。
(2)写出甲与NaOH溶液反应的离子方程式 ▲ 。另外,工业上常用甲与焦炭、氯气共热生成化合物丁和CO,而丁仅由两种元素组成,请写出该反应的化学方程式并标出电子转移的方向和数目 ▲ 。
(3)乙溶于氢氟酸后生成一种极强的二元酸和水。经分析该酸由3种元素组成,其中氟元素的质量分数为79.17%。请写出乙溶于氢氟酸的离子反应方程式 ▲ 。
(4)将固体X溶于适量的硫酸,往所得溶液中滴加NaOH浓溶液时,先出现蓝色絮状沉淀,继续滴加NaOH浓溶液并不断振荡,则沉淀消失形成蓝色溶液,若再滴加数滴乙二醇,可观察到溶液呈绛蓝色。可见,该蓝色絮状沉淀物具有 ▲ 。
A.酸性 B.碱性 C.两性 D.强还原性
请写出与乙二醇反应的化学方程式(无机反应物用蓝色絮状沉淀物的化学式表示)
▲ 。Ks*5u
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:填空题
氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。氨的水溶液中存在电离平衡,常用电离常数Kb和电离度α来定量表示其电离程度。Kb和α常用的测定方法:在一定温度时用酸度计测定一系列已知浓度氨水的pH,可得各浓度氨水对应的c(OH-),然后通过换算求得各对应的α值和Kb值。下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50 mL碱式滴定管、100mL烧杯、 0.10 mol·L-1 氨水
【实验数据】(不必填表格)
|
烧杯号 |
V氨水 (mL) |
V水(mL) |
c (NH3·H2O) (mol·L-1) |
c(OH-) |
Kb |
α |
|
1 |
50.00 |
0.00 |
|
1.34×10-3 |
|
|
|
2 |
25.00 |
25.00 |
|
9.48×10-4 |
|
|
|
3 |
5.00 |
45.00 |
|
4.24×10-4 |
|
|
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb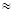 ▲ ,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系
▲ 。
▲ ,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系
▲ 。
(2)用0.10mol·L—1盐酸分别滴定20.00mL0.10mol·L—1的NaOH溶液和20.00mL0.10mol·L—1
氨水所得的滴定曲线如下:
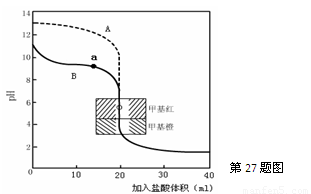
请指出盐酸滴定氨水的曲线为 ▲ (填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 ▲ 。
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= ▲ 。
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料。其总反应式为4NH3+3O2= 2N2+6H2O,正极上的电极反应式为O2+2H2O+4e—=4OH—,则负极上的电极反应式为 ▲ 。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:填空题
阿司匹林(乙酰水杨酸)已应用百年,成为医药史上三大经典药物之一,至今它仍是世界上应用最广泛的解热、镇痛和抗炎药,也是作为比较和评价其他药物的标准制剂。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成该物质,设计的合成路线为:
一、制备K
 s*5u
s*5u
二、提纯
方案1
方案2
主要试剂和产品的物理常数
|
名 称 |
相对分子质量 |
熔点或沸点(0C) |
水 |
醇 |
醚 |
|
水杨酸 |
138 |
158(熔点) |
微溶 |
易溶 |
易溶 |
|
醋酸酐 |
102 |
139.4(沸点) |
反应 |
可溶 |
易溶 |
|
乙酰水杨酸 |
180 |
135(熔点) |
微溶 |
可溶 |
微溶 |
请根据以上信息回答下列问题:
(1)①合成阿斯匹林时,还会生成一些副产品,其中有一种是高分子,为了分离此物质,方案1中加入A物质为 ▲ 溶液。
②本方案抽滤后进行洗涤,其具体操作是 ▲ 。
(2)方案2为改进的提纯方法,称为重结晶提纯法。
①该方案中步骤1除了选用乙酸乙酯外,还可选择下列哪些
试剂 ▲ 。
A. 乙醇 B. 蒸馏水 C. 乙醚
②步骤2回流的装置如图所示,写出仪器a的名称 ▲ ,使用温度计的目的是 ▲ ,冷凝水的流向为 ▲ 。

③方案2所得产品的有机杂质要比方案1少的原因是 ▲ 。
(3)该学习小组在实验中原料用量:2.0g水杨酸、5.0ml醋酸酐(ρ=1.08g·cm-3),
最终称量产品m=2.2g ,则乙酰水杨酸的产率为 ▲ 。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省台州市高三调考试题(理综)化学部分 题型:填空题
罗伯特·格拉布等三位科学家因在烯烃复分解反应研究方面取得了显著成就而荣获2005年诺贝尔化学奖。烯烃的复分解反应机理可视为双键断裂,换位连接,如:
CH2=CHR1 + CH2=CHR2
 CH2=CH2 + R1CH=CHR2
CH2=CH2 + R1CH=CHR2
已知: F是油脂水解产物之一,能与水任意比互溶;K是一种塑料;J的化学式为C9H14O6。物质转化关系如下图所示:

请回答下列问题:
(1)请写出下列物质的结构简式:A. ▲ ,J. ▲ 。
(2)写出 C → D的化学方程式: ▲ ,该反应的反应类型是 ▲ ,
G → B的反应类型是 ▲ 。
(3)A与A的所有烯烃同分异构体之间,通过烯烃复分解反应后形成的新烯烃有 ▲ 种结构;这些新烯烃和氯化氢在一定条件下发生加成反应,则其产物只有一种结构的新烯烃的结构简式为:CH2=CH2、 ▲ 、 ▲ 。
(4) 以G为原料经过一系列反应最终可制得乙酰乙酸乙酯(无色液体),通常状况下乙酰乙酸乙酯可逐渐转化为烯醇式 (达到平衡后烯醇式约占7%):

乙酰乙酸乙酯(酮式) (烯醇式)
已知FeCl3溶液可和烯醇式反应显紫色。某同学拟用5%的FeCl3溶液和Br2的CCl4溶液来证明上述平衡的存在,请简要描述实验过程和现象。
查看答案和解析>>
科目: 来源:2010-2011学年浙江省名校名师新编“百校联盟”交流高三联考(理综)化学部分 题型:选择题
化学与工农业生产、环境保护、日常生活等方面有广泛联系,下列叙述正确的是( )
A.棉花和木材的主要成分都是纤维素、蚕丝和人造丝的主要成分都是蛋白质
B.腌制熟食品时,添加少量亚硝酸钠,是为了使其味道更加美味可口
C.为了防止月饼等富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰
D.“神七”宇航员所穿出舱航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
查看答案和解析>>
科目: 来源:2010-2011学年浙江省名校名师新编“百校联盟”交流高三联考(理综)化学部分 题型:选择题
用NA表示阿伏加德罗常数。下列叙述正确的是 ( )
A.2.0 g重水(2H2O)中含有的质子数为1.0 NA
B.在电解食盐水的实验中,测得则阴极析出的气体的分子数为0.5NA,则电解后溶液的pH为14。
C.25℃时,1 L pH=14的氢氧化钠溶液中约含有6.02×l023个氢氧化钠分子
D.1mol白磷分子中所含共价键数为4NA
查看答案和解析>>
科目: 来源:2010-2011学年浙江省名校名师新编“百校联盟”交流高三联考(理综)化学部分 题型:选择题
下列叙述不正确的是 ( )
A.电解氧化铝生成的金属铝是在熔融液的下层
B.手机上用的锂离子电池属于二次电池
C.钢铁吸氧腐蚀的正极反应:4OH- —4e-=2H2O+O2
D.铁表面镀锌,铁作阴极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com