
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:选择题
下列有关叙述错误的是
A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸
B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
C.某反应△H>0,△S>0,该反应可能自发进行
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(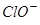 )=9.9×10-7mol/L.
)=9.9×10-7mol/L.
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:选择题
下列有关化学实验操作的叙述正确的是
A.在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液
B.向SO2溶液中分别滴加Ba(NO3)2、BaCl2、Ba(OH)2溶液,均产生BaSO3白色沉淀
C.向2.0mL浓度均为0.1mol/L的KCl和Kl混合溶液中滴加1~2滴0.01 mol/LAgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp大
D.分别电解熔融氯化镁和熔融氯化铝可以制取金属镁和金属铝
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:选择题
下列各溶液中,微粒的物质的量浓度关系正确的是
A.等体积、等物质的量浓度的CH3COONa与CH3COOH溶液混合:
2c(Na+)=c(CH3COO-)+c(CH3COOH)
B.0.1mol/L pH为10的NaHB溶液中:c(HB-)>c(B2-)>c(H2B)
C.常温下,将pH=10的NaOH溶液和pH=4的CH3COOH溶液等体积混合:
c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
D.等物质的量浓度的(NH4)2SO4和(NH4)2CO3溶液中的c(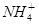 ):前者<后者
):前者<后者
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是 16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+H2SO4(80%)  Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
【注:80%H2SO4具有浓硫酸的特性】
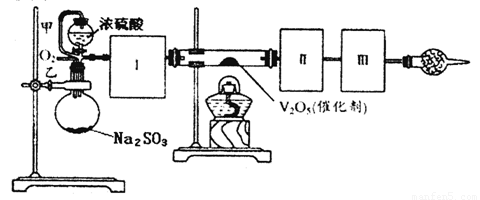
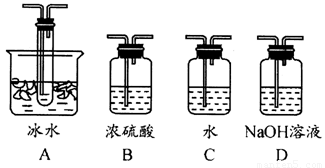
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~D装置中选择最合适的装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是___________、_____________、_____________。
(2)在实验中“加热催化剂”与“滴加浓硫酸”的操作,首先应采取的操作是___________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法。
①原因__________________________________________________.
验证方法________________________________________________.
②原因__________________________________________________.
验证方法________________________________________________.
(4)将足量SO2通入含1.0mol次氯酸的溶液中,有1.204×1024个电子转移,生成两种强酸,该反应的化学方程式为______________________________。
(5)用25.2gNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间将反应产生的SO2全部排出,测得装置Ⅲ增重了3.2g,则SO2的转化率为__________。
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
下图为一些物质间的相互转变关系,反应①在工业上可用来生产化合物C,反应⑤在工业上可生产化合物J(Na2FeO4),反应①、②、④和⑤均是在水溶液中进行的反应.常温下,D、E、G均是气体,B是无色液体;F的水溶液可作为杀菌消毒剂;H是一种铁矿石的主要成分,它由两种元素组成,且其中铁元素的质量分数为70%。
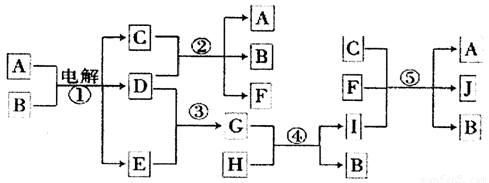
请回答下列问题:
(1)工业上利用反应①生产化合物C,得到化合物C的电极名称是______________。
(2)化合物F中阴离子的电子式为_______________。
(3)反应②的化学方程式为____________________。
(4)反应⑤的离子方程式为___________________________。
(5)高铁酸钠(Na2FeO4)既能杀菌消毒又是一种“绿色环保高效”的净水剂,其原因为:
①_______________________________________________________。
②_______________________________________________________。
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。

(1)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:某温度下,在容积为2L的密闭容器中,充入1molCO2和3.25molH2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间变化如右图所示:
①从反应开始到平衡,氢气的平均反应速率v(H2)=__________________________.
②下列措施中一定不能使CO2的转化率增大的是________________。
A.在原容器中再充入1molCO2 B.在原容器中再充入1molH2
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
E.缩小容器的容积 F.将水蒸气从体系中分离
(2)常温常压下,饱和CO2水溶液的pH=5.6,c(H2CO3)=1.5×10-5mol/L。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 +H+的电离平衡常数K=____________。(已知:10-5.6=2.5×10-6)。
+H+的电离平衡常数K=____________。(已知:10-5.6=2.5×10-6)。
(3)标准状况下,将4.48LCO2通入200mL1.5mol/L的NaOH溶液,所得溶液中离子浓度由大到小的顺序为_____________。
(4)如图是甲醇燃料电池(电解质溶液为KOH溶液)的
结构示意图,则a处通入的是_________(填“甲醇”或
“氧气”),其电极上发生的电极反应式为_____________。

(5)已知,常温下Ksp(AgCl)=2.0×10-10,Ksp(AgBr)=5.4×10-13. 向BaCl2溶液中加入AgNO3和KCl,当两种沉淀共存时,溶液中c(Br-)和c(Cl-)的比值为___________。
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素,其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的+3价离子的3d能级为半充满状态。(答题时用ABCDE对应的元素符号表示)
(1)A的氢化物A2H2分子的空间构型为__________,其中心原子采取的杂化形式为___________,分子中含有___________个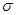 键,__________π键。
键,__________π键。
(2)写出化合物DC的电子式_______,E原子的核外电子排布式________。
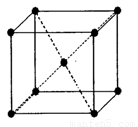
(3)由E元素形成的金属的晶胞结构如右图,则该晶胞中含有金属原子的数目为_______________。
(4)化合物E(CO)5常温下为液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于__________(填晶体类型)。
查看答案和解析>>
科目: 来源:2010-2011学年河南省商丘市高三第二次模拟考试(理综)化学部分 题型:填空题
棕榈科植物槟榔的干燥成熟种子可提取多种有机物,其中之一是异四氢烟酸,它具有镇痛和麻醉作用,异四氢烟酸也可通过实验室合成,其中一种合成路线如图所示:
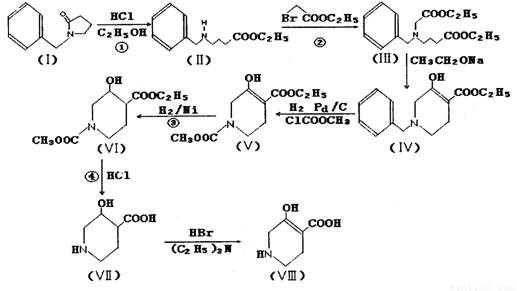
回答下列问题:
(1)上述转化中的①、③、③、④属于取代反应的是______________(选填序号)。
(2)有机物Ⅳ中含有多种官能团,试写出两种官能团的名称_____________。
(3)有机物Ⅲ在乙醇钠作用下生成的另一种有机物是_____________。
(4)有机物Ⅷ(异四氢烟酸)可以通过加聚反应生成高分子化合物,写出该反应的
化学方程式:_____________________________________。
(5)X是有机物Ⅷ的一种同分异构体,且符合下列转化关系和条件:
写出符合此转化关系和条件的X的结构简式________________________。
查看答案和解析>>
科目: 来源:2010-2011学年河南省高三模拟考试(理综)化学部分 题型:选择题
山梨酸是一种常见的食品添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为 CH3—CH=CH—CH=CH—COOH。下列关于山梨酸的叙述不正确的是
A.山梨酸易溶于乙醇
B.山梨酸能和乙醇反应生成酯
C.山梨酸能与氢气发生加成反应
D.1mol山梨酸能和金属钾反应生成1mol氢气
查看答案和解析>>
科目: 来源:2010-2011学年河南省高三模拟考试(理综)化学部分 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1 mol Na2O2固体中含离子总数为4NA
B.等物质的量的N2和CO所含分子数均为NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com