
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:选择题
4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1∶2,X2+ 和Z-离子的电子数之差为8。下列说法不正确的是
A.W与Y通过离子键形成离子化合物
B.元素原子半径从大到小的顺序是X、Y、Z
C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构
D.W、Y、Z元素最高价氧化物对应的水化物中酸性最强的元素是Z
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:选择题
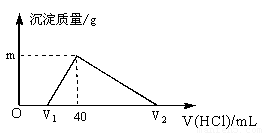
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是[来源:ZX
 XK]
XK]
A.原合金质量为0.92g[来源:Zxxk.Com]
B.产生氢气的体积为896mL(标准状况下)
C.图中m的值为1.56
D.图中V2为60
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
已知:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
2NH3(g)△H=-92.4kJ/mol,这是目前普遍使用的人工固氮的方法。请回答下列问题:
(1)450℃时,往一个2L的密闭容器中充入2. 6mol H2和1mol N2, 反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
|
时间/min |
5 |
10 |
15 |
20 |
25 |
30 |
|
c(NH3)/mol·L—1 |
0.08 |
0.14 |
0.18 |
0.20 |
0.20 |
0.20 |
①5 min内,消耗N2的平均反应速率为_______________,此条件下该反应的化学平衡常数K=_______________;反应达到平衡后,若往平衡体系中加入H2、N2和NH3各2mol,此时该反应的v(N2)正_______________v(N2)逆(填写“>”、“=”或“<”=)。
②下列各项能作为判断该反应达到化学平衡状态的依据是__________(填序号字母)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.v(N2)正=3v(H2)逆 C.容器内压强保持不变
D.混合气体的密度保持不变 E.容器内混合气体的平均分子量不变
③若改变某一条件,达新平衡时n(H2)=1.60mol ,下列说法正确的是_____________。
A.平衡一定正向移动 B.可能是向容器中加入了一定量的H2气体
C.可能是降低了容器的温度 D.可能是缩小了容器的体积
(2)450℃时,在另一密闭容器中进行上述合成氨的反应,各物质的起始浓度和平衡浓度如下表所示:
|
|
N2 |
H2 |
NH3 |
|
起始浓度(mol/L) |
0.2 |
0.3 |
0.2 |
|
平衡浓度(mol/L) |
a |
b |
c |
请回答:
①各物质的平衡浓度可能是_______________.
A.c=0.5mol/L B.b=0.5mol/L C.c=0.4mol/L D.a=0.3mol/L
②a的取值范围是:_______________.
③请用数学表达式表示下列量之间的关系:
(I)a与b的关系:_______________。
(Ⅱ)a、b、c的关系:_______________。
(3) 根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水可发生下列反应:2N2(g)+6H2O(l)  4NH3(g)+3O2(g),此反应的△S__________0(填“
4NH3(g)+3O2(g),此反应的△S__________0(填“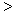 ”、 “
”、 “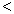 ”或“=”), △H=_____________。
”或“=”), △H=_____________。
(已知:H2的燃烧热为285.8 kJ/mol)
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
D、E为中学化学常见的单质,在一定条件下C、D间能发生反应。各物质转化关系如下图:
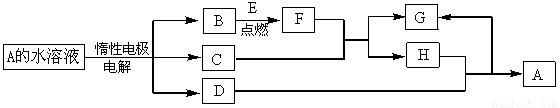
(1)B的同素异形体的名称为:_____________;H的化学式为:_____________。
(2)已知E的燃烧热为QkJ/mol,试写出表示E燃烧热的热化学方程式_____________。
(3)用惰性电极电解A 溶液的阳极反应式为:_____________。
(4)检验H和G的混合溶液中含有G的阳离子的试剂可以是:_____________。
a.氯水和KSCN溶液 b.氢氧化钠溶液 c. 酸性KMnO4溶液
(5)用惰性电极电解一定浓度的A溶液,通电一段时间后,向所得溶液中加入9.8g含A中金属阳离子的弱碱固体后恰好恢复到电解前的浓度和pH。则电解过程中转移电子的物质的量为_____________mol, 收集到标准状况下的气体体积为_____________。
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
某化学活动小组设计如图所示装置(部分夹持装置已略去)实验,以探究潮湿的Cl2与Na2CO3反应的产物。
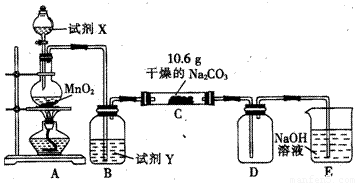
(1)写出装置A中发生反应的化学方程式:__________________________。
(2)写出试剂Y的名称:_______________________________________。
(3)将C中反应后的固体物质分成两等份分装于两支试管中,
①向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,写出产生此现象的离子方程式: ______________;由此现象推断固体产物中含有_____________(填化学式,下同);
②向另一支试管中滴加过量的稀硝酸,有无色无味的气体产生,溶液澄清,再向溶液滴加过量的AgNO3溶液,溶液变浑浊,经过滤、洗涤、干燥,得到7.175g固体,由此现象推断固体产物中含有_____________。
(4)已知C中有0.1molCl2参加反应,D中收集到的气体是氯的一种氧化物。结合(2)中现象及数据可推知,C中反应的化学方程式为__________________________。
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体的生产流程,其流程示意图如下:

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时的pH见下表:
|
离子 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe2+ |
7.6 |
9.7 |
|
Fe3+ |
2.7 |
3.7 |
|
Al3+ |
3.8 |
4.7 |
|
Mn2+ |
8.3 |
9.8 |
请回答下列问题:
(1)写出浸出过程中主要反应的化学方程式: ________________________。
(2)写出氧化过程中主要反应的离子方程式: ______________________。
(3)在氧化后的液体中加入石灰浆,并用pH试纸测定调节pH,pH应调节范围是____________。
(4)滤渣的主要成分有_________________________________________。
(5)下列各组试剂中,能准确测定尾气中SO2含量的是__________。(填编号)
a. NaOH溶液、酚酞试液 b. 稀H2SO4酸化的KMnO4溶液
c. 碘水、淀粉溶液 d. 氨水、酚酞试液
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
已知X、Y和Z三种元素的原子序数之和等于48。X的一种1:1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单位为正方体(如右图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。

⑴Y在周期表中位于______________;Z4+的核外电子排布式为______________;
⑵X的该种氢化物分子构型为___________,X在该氢化物中以_____________方式杂化。X和Y
形成的化合物的熔点应该_____________(填“高于”或“低于”)X氢化物的熔点。
⑶①制备M的化学反应方程式是________________________________________;
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的______;
③在M晶体中,Z4+的氧配位数为________;
④已知O2-半径为1.40×10-10 m,则Z4+半径为___________m。
查看答案和解析>>
科目: 来源:2010-2011学年江西省协作体高三第二次联考(理综)化学部分 题型:填空题
芳香族化合物A有如下图的转化关系:
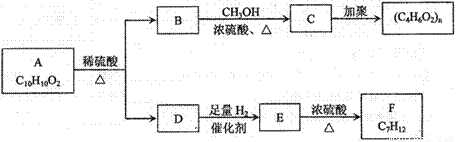
已知D能与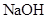 溶液反应,E转化为F时,产物只有一种结构,且能使溴的四氯化碳溶液褪色。请回答下列问题:
溶液反应,E转化为F时,产物只有一种结构,且能使溴的四氯化碳溶液褪色。请回答下列问题:
(1)B的分子式是_____________
(2)A、F的结构简式 A ___________ F __________
(3)写出B→C、E→F的化学反应方程式,并注明反应类型
B→C:_____________________________________________( )
E→F:_____________________________________________( )
(4)符合下列3个条件的A的同分异构体有多种
①苯环含有对二取代结构 ②遇FeCl3溶液不变色
③能发生银镜反应
请写出其中任意一种的结构简式________________________________________
查看答案和解析>>
科目: 来源:2010-2011学年江西省联盟高三第一次联考理综化学部分 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.250C时,pH = 13的1L Ba(OH)2溶液中含有OH-数目为0.1NA
B.200mL 5mol·L-1Na2S溶液中,含NA个S2-
C.常温下,pH=12的1L氨水中含有的NH3·H2O分子数是0.01 NA
D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com