
科目: 来源:不详 题型:单选题
| A.水溶液中或融熔状态下能导电的化合物是电解质,已知化合物SO3的水溶液能导电,由此判断SO3属于电解质 |
| B.一定温度和压强下,各种气态物质体积的大小,主要由气体的物质的量决定 |
| C.2mol水的摩尔质量与1mol水的摩尔质量之比为2:1 |
| D.在化学反应中某元素化合价只升高,则反应过程中该元素被还原了 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
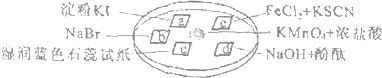
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变化,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性:Fe2+>Cl- |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:内江三模 题型:问答题
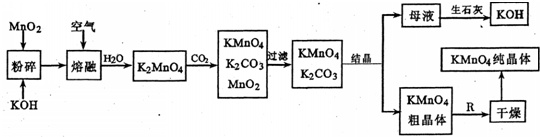
查看答案和解析>>
科目: 来源:福建省期中题 题型:单选题
查看答案和解析>>
科目: 来源:不详 题型:填空题
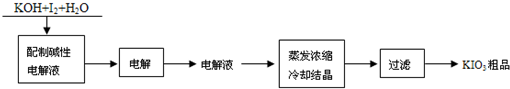
查看答案和解析>>
科目: 来源:安徽模拟 题型:问答题
| 放电 |
| 充电 |
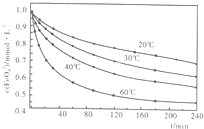
查看答案和解析>>
科目: 来源: 题型:
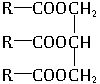 (烃基R中不含三键)。0.1molA与溶有96g液溴的四氯化碳恰好完全反
(烃基R中不含三键)。0.1molA与溶有96g液溴的四氯化碳恰好完全反查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com