
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
对于Zn(s)+H2SO4(l)=ZnSO4(l)+H2(g);ΔH <0 的化学反应下列叙述不正确的是( )
A.反应过程中能量关系可用右图表示

B.若将该反应设计成原电池锌为负极
C.ΔH的值与反应方程式的计量系数无关
D.若将其设计为原电池当有32.5g锌溶解时,
正极放出气体一 定为11.2L
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:
C2H5OH +3O2 =2CO2 +3H2O,电池示意如图。

下列说法不正确的是( )
A.a极为电池的负极
B.电池工作时电流由b极沿导线经灯泡再到a极
C.电池正极的电极反应为:4H+ + O2 + 4e- =2H2O
D.电池工作时,1mol乙醇被氧化时就有6mol电子转移
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
有人设计出利用CH4和O2的反应,用铂电极在KOH溶液中构成原电池。电池的总反应类似于CH4在O2中燃烧,则下列说法正确的是( )
①每消耗1molCH4可以向外电路提供8mole-
②负极上CH4失去电子,电极反应式CH4+10OH--8e-=CO32-+7H2O
③负极上是O2获得电子,电极反应式为 O2+2H2O+4e-=4OH-
④电池放电后,溶液pH不断升高
A.①② B.①③ C.①④ D.③④
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量。已知白磷和P4O6的分子结构如右图所示

现提供以下化学键的键能:P—P
198kJ·mol—1、P—O 360kJ·mol—1、O=O为:498 kJ·mol—1。则反应P4(白磷)+3O2 P4O6的反应热△H为( )
A.-1638 kJ/mol B.+1638 kJ/mol
C.-126 kJ/mol D.+126 kJ/mol
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,生成N2和水蒸气。已知:N2(g)+2O2(g)====N2O4(g) ΔH=+8.7 kJ·mol-1
N2H4(g)+O2(g) ====N2(g)+2H2O(g) ΔH=-534.0 kJ·mol-1
下列表示肼跟N2O4反应的热化学方程式,正确的是( )
A.2N2H4(g)+N2O4(g) ====3N2(g)+4H2O(g) ΔH=-542.7 kJ·mol-1
B.2N2H4(g)+N2O4(g) ====3N2(g)+4H2O(g) ΔH=-1 059.3 kJ·mol-1
C.N2H4(g)+1/2 N2O4(g) ====3/2N2(g)+2H2O(g) ΔH=-1 076.7 kJ·mol-1
D.2N2H4(g)+N2O4(g) ====3N2(g)+4H2O(g) ΔH=-1 076.7kJ·mol-1
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
.已知H2(g)+Br2(l)=2HBr(g),ΔH =-72kJ·mol-1,蒸发1mol Br2(l)需要吸收的能量为30kJ,其它相关数据如下表:
|
|
H2(g) |
Br2(g) |
HBr(g) |
|
1mol分子中的化学键断裂时需要吸收的能量/KJ |
436 |
a |
369 |
则表中a为( )
A.404 B.260 C.230 .200
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O=Zn(OH)2+Mn2O3,下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极反应式为: 2MnO2+H2O+2e-= Mn2O3+2OH-
C.电池工作时,负极附近pH降低
D.正极是水电离出的H+得到电子
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
氢氧燃料电池是一种高性能电池,总反应为2 H2 + O2 = 2 H2O,电解质溶液为KOH溶液,下列有关该电池的叙述中不正确的是( )
A.H2为负极,O2为正极 B.工作时电解质溶液的PH不断增大
C.负极反应:2H2-4e- +4OH-=4H2O D.正极反应:O2 + 4e- +2 H2O=4OH-
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流。电池总反应为:4Al+3O2+6H2O=4Al(OH)3,下列说法不正确的是( )
A.正极反应为:O2+2H2O+4e-=4OH-
B.电池工作时,电流由铝电极沿导线流向铂电极
C.该电池通常只需要更换铝板就可继续使用
D.以网状的铂为正极,可增大与氧气的接触面积
查看答案和解析>>
科目: 来源:2011-2012年福建省福州市高二上学期第一次月考化学试卷 题型:选择题
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O
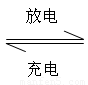 Cd(OH)2 + 2Ni(OH)2
,
Cd(OH)2 + 2Ni(OH)2
,
有关该电池的说法正确的是( )
A.放电时正极反应: NiOOH + H2O + e- == Ni(OH)2 + OH-
B.放电过程电能转化为化学能
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH—向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com