
科目: 来源:2011-2012年学山东省高三上学期模块检测化学试卷 题型:填空题
由熔盐电解法获得的粗铝含有一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去。
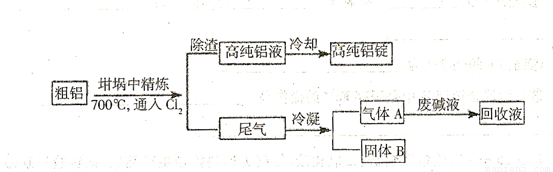
(注:NaCl熔点为801℃; 在181℃升华)
在181℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为① 和② 。
(2)将 连续通人坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除
连续通人坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除 外还含有
,固态杂质粘附于气泡上,在熔体表面形定浮渣,浮渣中肯定存在
。
外还含有
,固态杂质粘附于气泡上,在熔体表面形定浮渣,浮渣中肯定存在
。
(3)在用废碱液处理A的过程中,所发生反应的离子方程式为
。
查看答案和解析>>
科目: 来源:2011-2012年学山东省高三上学期模块检测化学试卷 题型:填空题
甲、乙两同学为探究 与可溶性钡的强酸盐能否反应生成白色
与可溶性钡的强酸盐能否反应生成白色 沉淀,用下图所示装置进行实验(夹持装置和A中加执装置已略,气密性已检验)
沉淀,用下图所示装置进行实验(夹持装置和A中加执装置已略,气密性已检验)

实验操作和现象:
|
操作 |
现象 |
|
关闭弹簧夹,滴加一定量浓硫酸,加热 |
A.中有白雾生成,铜片表面产生气泡 B.中有气泡冒出,产生大量白色沉淀 C.中产生白色沉淀,液面上方略显红棕色并逐渐消失 |
|
打开弹簧夹,通入 |
|
|
从B、C中分别取少量白色沉淀,加稀盐酸 |
均未发现白色沉淀溶解 |
(1)A中反应的化学方程式是 。
(2)C中白色沉淀是 。
(3)C中液面上方生成红棕色气体的化学方程式是 。
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲同学认为是空气中的氧气参与反应,乙同学认为是白雾(硫酸酸雾)参与反应。
①为证实各自的观点,在原实验基础上;甲同学在原有操作之前通 一段时间,目的是
。乙同学在A、B间增加盛有饱和
一段时间,目的是
。乙同学在A、B间增加盛有饱和 溶液的洗气瓶D,D中反应的离子方程式是
。
溶液的洗气瓶D,D中反应的离子方程式是
。
②各自进行实验,B中现象:
|
甲 |
大量不溶于稀盐酸的白色沉淀 |
|
乙 |
少量不溶于稀盐酸的白色沉淀 |
用离子方程式解释乙同学观察到的实验现象
(不必配平)。
(5)若将(4)中两同学的方案进行联合试验,发现B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是 。
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
二氧化硫与氧气的反应为:2SO2(g)+ O2(g) 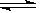 2 SO3
(g); △H <0, 该反应在硫酸工业生产中应采取的适宜条件是(
)
2 SO3
(g); △H <0, 该反应在硫酸工业生产中应采取的适宜条件是(
)
A.低温、高压、催化剂 B. 适宜的温度、高压、催化剂
C.低温、常压、催化剂 D. 适宜的温度、常压、催化剂
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
可逆反应2HI(g)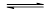 I2(g)+H2(g)在密闭容器中进行,当下列中的四项中的某项不随时间变化时,不能说明反应达到平衡的是( )
I2(g)+H2(g)在密闭容器中进行,当下列中的四项中的某项不随时间变化时,不能说明反应达到平衡的是( )
A.各组分的物质的量 B.混合物的温度 C.容器内压强 D.混合气体的颜色
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
增大压强能使下列化学反应的平衡向正反应方向移动的是( )。
A.C(s)+CO2(g) 2CO(g)
B.3H2(g)+N2(g)
2CO(g)
B.3H2(g)+N2(g) 2NH3(g)
2NH3(g)
C.H2(g)+I2(g) 2HI(g)
D.C(s)+H2O(g)
2HI(g)
D.C(s)+H2O(g) CO(g) + H2(g)
CO(g) + H2(g)
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
对于反应A + B = C,下列条件的改变一定使化学反应速率加快的是( )
A.升高体系的温度 B.增加体系的压强
C.增大C的物质的量浓度 D.增加A的物质的量
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
下列说法,你认为不正确的是( )。
A.平衡常数随温度的改变而改变
B.对于密闭容器中反应2SO2+O2 2SO3,2体积SO2与足量O2反应,能生成2体积SO3
2SO3,2体积SO2与足量O2反应,能生成2体积SO3
C.合成氨反应中使用催化剂,降低了反应所需要的活化能。
D.反应H2(g)+I2(g)  2HI(g) 在450℃时,其平衡常数为49;则反应
2HI(g) 在450℃时,其平衡常数为49;则反应
HI(g)  1 ∕ 2 H2(g) +1 ∕ 2 I2(g) 在450℃时的平衡常数为1 ∕ 7
1 ∕ 2 H2(g) +1 ∕ 2 I2(g) 在450℃时的平衡常数为1 ∕ 7
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
下列情况下,反应速率相同的是 ( )
A.等体积0.1 mol/L HCl和0.1 mol/L CH3COOH分别与0.2 mol/L NaOH溶液反应
B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
下列措施或事实能用勒沙特列原理解释的是( )
A.在合成氨(正反应是放热)的反应中,升温有利于氨的合成
B.H2、I2、HI三者的平衡混合气,加压(缩小容器体积)后颜色变深
C.钢铁在潮湿的空气中更容易生锈
D.氯气可以用排饱和食盐水的方法收集
查看答案和解析>>
科目: 来源:2011-2012年学福建省高二上学期期中考试化学试卷 题型:选择题
四个体积相同的密闭容器中在一定的条件下发生反应:2SO2+O2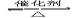 2SO3,反应开始时,反应速率由大到小排列顺序正确的是( )
2SO3,反应开始时,反应速率由大到小排列顺序正确的是( )
|
容器 |
温度 |
SO2(mol) |
O2(mol) |
催化剂 |
|
甲 |
5000C |
10 |
5 |
- |
|
乙 |
5000C |
8 |
5 |
V2O5 |
|
丙 |
4500C |
8 |
5 |
- |
|
丁 |
5000C |
8 |
5 |
- |
A.乙>甲>丁>丙 B.乙>甲>丙>丁 C.甲>乙=丁>丙 D.乙>甲>丙=丁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com