
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
某温度下,在固定容积的容器中,可逆反应A(g)+3B(g) 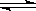 2C(g)达到平衡,此时测得n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向该容器中再充入A、B和C,下列叙述正确的是
2C(g)达到平衡,此时测得n(A)∶n(B)∶n(C)=2∶2∶1。若保持温度不变,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向该容器中再充入A、B和C,下列叙述正确的是
A、 刚充入时反应速率υ正减少,υ逆增大 B、 平衡不发生移动
C、 平衡向逆反应方向移动 D、 物质C的质量分数增大
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
①NaOH固体 ②H2O ③NH4Cl固体 ④CH3COONa固体 ⑤NaNO3固体 ⑥KCl溶液
A、②④⑥ B、①② C、②③⑤ D、②④⑤⑥
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A、生成了一种强酸弱碱盐 B、弱酸溶液和强碱溶液反应
C、强酸溶液和强碱溶液反应 D、二元强酸溶液和一元强碱溶液反应
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
下列离子方程式中正确的是
A、 氢氧化钠溶液吸收过量的二氧化碳 OH-+CO2 = HCO3-
B、 亚硫酸氢铵溶液与足量氨水反应 HSO3-+ OH-= SO32-+ H2O
C、 氯气通入冷水中 Cl2 +H2O = Cl- +ClO- +2H+
D、 碳酸镁悬浊液中加醋酸 CO32-+2CH3COOH = 2CH3COO-+CO2↑+H2O
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
室温下pH相同,体积也相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A、 加水稀释2倍后,两溶液的pH均减小
B、 使温度都升高20℃后,两溶液的pH均不变
C、 加适量的醋酸钠晶体后,两溶液的pH均增大
D、 加足量的锌充分反应后,两种酸产生的氢气一样多
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
下列说法正确的是
①CH3COONa、BaSO4都是强电解质; ②中和滴定过程中,应注视锥形瓶内溶液颜色的变化,以准确把握滴定终点;③测定溶液的PH值时,用玻璃棒蘸取少量溶液点在湿润的pH试纸上再与标准比色卡对照;④ 0.1 mol·L-1 NaOH溶液与0.1 mol·L-1 Ba(OH)2 溶液的PH相同;⑤日用铝制品表面覆盖着氧化膜,对内部金属起保护作用。[来源:]
A、①②④ B、①②⑤ C、②③⑤ D、③④⑤
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
T ℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是
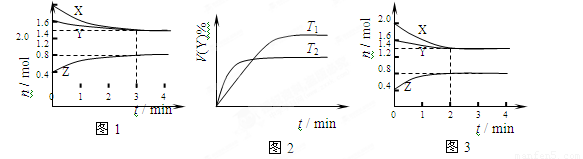
A.容器中发生的反应可表示为:3X(g)+Y(g)  2Z(g)
2Z(g)
B.保持其他条件不变,升高温度,化学平衡向逆反应方向移动
C.反应进行前4 min内,用X表示的反应速率 v(X)=0.075mol•(L•min) -1
D.若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:选择题
下列各组热化学方程式中,△H前者大于后者的是
①C(s)+O2(g)=CO2(g); C(s)+1/2O2(g)=CO(g)
②S(s)+O2(g)=SO2(g); S(g)+O2(g)=SO2(g)
③H2(s)+1/2O2(g)=H2O(l); 2H2(g)+O2(g)=2H2O(l)
④2KOH (aq) +H2SO4(aq)=K2SO4(aq)+2H2O (l);
2KOH (aq) +H2SO4(浓)=K2SO4(aq)+2H2O (l)
A、①③ B、②④ C、②③④ D、①②③
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:填空题
(4分)在发射“神舟”七号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:
N2H4(l)+2H2O2(l)===N2(g)+4H2O(g) ΔH = -641.6 kJ/mol
H2O(l)===H2O(g) ΔH = +44 kJ/mol
若用3.2 g液态肼与足量过氧化氢反应生成氮气和液态水,则整个过程中转移的电子的物质的量为__________,该反应的热化学方程式为 。
查看答案和解析>>
科目: 来源:2013届黑龙江省高二上学期期中考试化学(理)试卷 题型:填空题
(16分)炼金废水中含有络离子[Au(CN)2]-,它能电离出有毒的CN-,当CN-与H+结合时生成剧毒的HCN。完成下列问题:
(1)HCN的水溶液酸性很弱,则HCN电离方程式为_________________,NaCN的水溶液呈碱性是因为_________________(用离子方程式表示)。
(2)室温下,如果将0.2mol NaCN和0.1mol HCl全部溶于水,形成混合溶液(假设无损失),①__ _和_ __两种粒子的物质的量之和等于0.2mol。②_ __和_ __两种粒子的物质的量之和比H+多0.1mol。
(3)已知某溶液中只存在OH-、H+、Na+、CN-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A、c(CN-)>c(Na+)>c(H+)>c(OH-) B、c(Na+)>c(CN-)>c(OH-)>c(H+)
C、c(CN-)>c(H+)>c(Na+)>c(OH-) D、c(CN-)>c(Na+)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,上述离子浓度大小顺序关系中正确的是(填序号) 。
②若上述关系中C是正确的,则溶液中溶质的化学式是_ _和_ 。
③若该溶液中由体积相等的稀HCN溶液和NaOH溶液混合而成,且恰好呈中性,则混合前
c(HCN) c(NaOH)(填“>”、“<”、或“=”下同),
混合后溶液中c(Na+)与c(CN-)的关系c(Na+) c(CN-)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com