
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:选择题
下列用来表示物质变化时的化学用语中,正确的是
A.氢硫酸溶液显酸性的主要原因:H2S 2H++ S2–
2H++ S2–
B.用稀氨水吸收H2S:NH3·H2O + H2S === NH4HS+ H2O
C.Na2CO3溶液显碱性的主要原因:CO32-+ 2H2O  H2CO3 + 2OH–
H2CO3 + 2OH–
D.CH3COOH(aq) + NaOH(aq) === CH3COONa (aq) + H2O(l) ΔH= –57.3kJ/mol
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:选择题
下列说法错误的是
A.25℃时,pH=9的NaHA溶液中: c(A )< c(H2A)
)< c(H2A)
B.25℃时,pH=9的NaHA溶液中: c(H+)十c(H2A)= c(OH–) + c(A2–)
C.25℃时,0.1 mol·L-1NaF溶液与0.1 mol·L-1CH3COOK溶液: c(F–)> c(CH3COO–)
(已知酸性HF>CH3COOH)
D.25℃时,pH相等的NaF溶液与CH3COOK溶液: c(NaF)< c(CH3COOK)
(已知酸性HF>CH3COOH)
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:填空题
(10分)硫酸是工业生产中最为重要的产品之一。在催化反应室里进行的反应为:
2SO2(g)+O2(g) 2SO3(g) ΔH= –196.6 kJ·mol-1
2SO3(g) ΔH= –196.6 kJ·mol-1
(1)该反应发生的条件通常是400~500℃、 和 。
(2)SO3在 (填设备名称)中用 (填试剂名称)吸收。
(3)研究SO2 、NO2、CO等大气污染气体的处理具有重要意义。
已知: 2NO(g)+O2(g) 2NO2(g)
ΔH= –113.0 kJ·mol-1
2NO2(g)
ΔH= –113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
kJ·mol-1。
SO3(g)+NO(g)的ΔH=
kJ·mol-1。
一定条件下,将NO2与SO2以物质的量之比1:2置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2的物质的量之比为1:6,则平衡常数K= 。
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:填空题
(10分)A、B、C、 D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液 、盐酸中的一种。常温下:
①浓度均为0.1mol·L-1的A和C溶液,pH:A<C<7;
②将1 L pH=3的A溶液分别与0.001mol·L-1 xL B溶液、0.001mol·L-1 yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是 (填化学式)溶液;
(2)②中1LpH=3的A溶液与0.001mol·L-1 xL B溶液充分反应至中性,所得溶液中各种离子的物质的量浓度由大到小的顺序为 。
(3)常温下,等体积且等物质的量浓度的C溶液和 D溶液充分混合后所得溶液的pH
7(填“>”、“<”或“=”),用离子方程式解释其原因 。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是 (填写序号)。
①开始反应时的速率A>C ②反应所需要的时间C>A
③参加反应的锌粉物质的量A=C ④A溶液里有锌粉剩余
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:填空题
(10分)利用天然气合成氨的工艺流程示意图如下:
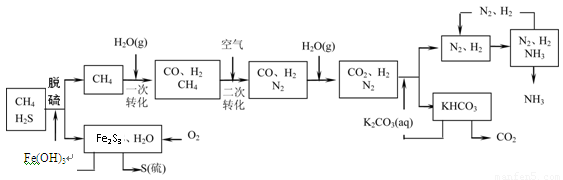
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是 。
(2)图中CH4的第一次转化过程中的化学方程式是 。
(3)整个流程有三处循环,一是K2CO3(aq)循环,二是N2和H2循环,三是 (填化学式)循环。
(4)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)。
a.熵增原理 b.勒夏特列原理 c.酸碱中和原理
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:实验题
(16分)纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
(1)制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,该水解反应的化学方程式为 。再经过滤、水洗除去其中的Cl–,再烘干、焙烧除去水分得到粉体TiO2 。检验TiO2·xH2O中Cl–是否被除净的方法是 。
(2)用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是 ;
②滴定终点的现象是 。
③滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为 。
④下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果 。
若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果 。
查看答案和解析>>
科目: 来源:2013届重庆市高二上学期期中考试化学试卷 题型:填空题
(11分)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
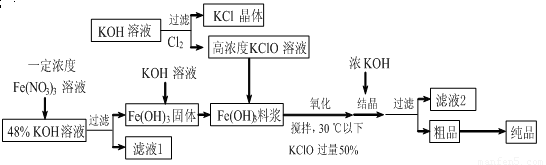
(1)上述氧化过程中,发生反应的离子方程式是: ,控制反应温度30℃以下的原因是: 。
(2)结晶过程中加入浓KOH溶液的作用是: 。
(3)根据图1、图2回答:为了获取更多的高铁酸钾,铁盐的质量分数应控制在 附近、反应时间应控制在 。
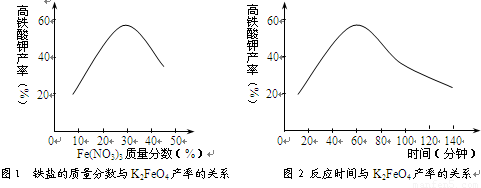
查看答案和解析>>
科目: 来源:2013届陕西省咸阳市高二上学期期中考试化学试卷 题型:选择题
下列叙述正确的是( )
A.强电解质都是离子化合物,因此NaCl是离子化合物
B.醋酸溶液的导电能力可能比硫酸溶液强
C.SO3溶于水,其水溶液能导电,故SO3是电解质
D.硫磺是单质,不导电,因此硫磺是非电解质
查看答案和解析>>
科目: 来源:2013届陕西省咸阳市高二上学期期中考试化学试卷 题型:选择题
下列描述违背化学原理的是( )
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.电解饱和食盐水时,阳极的电极反应式为:2Cl- -2e-= Cl2 ↑
查看答案和解析>>
科目: 来源:2013届陕西省咸阳市高二上学期期中考试化学试卷 题型:选择题
广义的水解观点认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别离解成两部分,然后两两重新组合成新的物质。根据上述观点,说法不正确的是( )
A.BaO2的水解产物是Ba(OH)2和H2O2 B.PCl3的水解产物是HClO和H3PO4
C.A14C3的水解产物是Al(OH)3和CH4 D.CH3COCl的水解产物是两种酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com