
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:选择题
已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O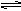 ?HCl+HClO;HClO
?HCl+HClO;HClO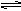 ?H++ClO-,达到平衡后,要使HClO的浓度增大,可加入下列物质:
?H++ClO-,达到平衡后,要使HClO的浓度增大,可加入下列物质:
A.SO2 B.NaHCO3 C.HCl D.NaOH
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:选择题
在一支25 mL的酸式滴定管中盛入0.1 mol/L HCl溶液,其液面恰好在5mL刻度处。若把滴定管内溶液全部放入烧杯中,再用0.1 mol/L NaOH溶液进行中和,则所需NaOH溶液的体积是:
A.等于5 mL B.小于20 mL C.等于20 mL D.大于20 mL
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:实验题
(12分)进行中和热的测定的装置如图所示。回答下列问题:

(1)从实验装置中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)利用该装置测得的中和热数值 (填“偏大、偏小、无影响”)
(4)某研究小组将装置完善后,把V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示
(实验中始终保持V1+V2=50 mL)。回答下列问题:
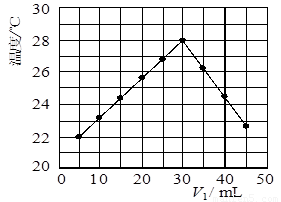
①研究小组做该实验时环境温度 (填“高于”、“低于”或“等于”)22 ℃。
②由题干及图形可知,V1/V2= : 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:实验题
(7分)实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数约为82.0%,为了验证其纯度,用浓度为0.2 mol/L的盐酸进行滴定,试回答下列问题:
(1)托盘天平称量5.0 g固体试剂,用500 mL容量瓶中配成待测液备用。
(2)将标准盐酸装在已经润洗过的25.00 mL酸式滴定管中,调节液面位置在 处,并记下刻度。
(3)取20.00 mL待测液,待测定。用甲基橙试剂作指示剂时,滴定到溶液颜色由 刚好至 色时为止。
(4)滴定达终点后,记下盐酸用去20.00 mL,计算NaOH的质量分数为 。
(5)试分析滴定误差可能由下列哪些实验操作引起的 。
A.转移待测液至容量瓶时,未洗涤烧杯
B.酸式滴定管用蒸馏水洗涤后,直接装盐酸
C.滴定时,反应容器摇动太激烈,有少量待测液溅出
D.滴定到终点时,滴定管尖嘴悬有液滴
E.读滴定管开始时仰视,读终点时俯视
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:填空题
(7分)在10℃和2×105Pa的条件下,反应aA(g) + bB(g)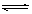 cC(g)建立平衡后再逐步增大体系的压强(温度不变)。下表列出了不同压强下反应建立平衡时物质A的浓度:
cC(g)建立平衡后再逐步增大体系的压强(温度不变)。下表列出了不同压强下反应建立平衡时物质A的浓度:
|
压强(Pa) |
2×105 |
4×105 |
8×105 |
|
A的浓度(mol/L) |
0.085 |
0.15 |
0.40 |
根据表中数据回答:
(1)压强从2×105Pa增加到4×105Pa时,平衡向 反应方向移动(填“正”、“逆”)。
(2)压强从4×105Pa增加到8×105Pa时,平衡向 反应方向移动(填“正”、“逆”),
可能原因是 。
(3)在10℃和2×105Pa的条件下,能作为该反应达到化学平衡状态的依据是 。
a.容器中气体的密度不变 b.混合气体中c(A)不变
c.v正(A )·b=v逆(B) ·a d.混合气体的平均相对分子量不变
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:填空题
(6分)已知T℃、P kPa时,在容积为V L密闭容器内充有1 mol A和1 mol B.保持恒温恒压,使反应:A(g)+B(g)  C(g)
达到平衡时,C的体积分数为40%。试回答有关问题:
C(g)
达到平衡时,C的体积分数为40%。试回答有关问题:
(1)欲使温度和压强在上述条件下恒定不变,在密闭容器内充入2 mol C,则反应达到平衡时,容器的容积为___________,C的体积分数为_________.
(2)若另选一容积固定不变的密闭容器,仍控制温度为T℃,使1 mol A和1 mol B反应达到平衡状态时,C的体积分数仍为40%,则该密闭容器的容积为_________.
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:填空题
(8分)常温下将0.2 mol/L HCl溶液与0.2 mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)①混合溶液中由水电离出的c(H+)________HCl溶液中由水电离出的c(H+)。(填“>”、“<”或“=”)
②求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Cl-)-c(M+)=__________mol/L;c(H+)-c(MOH)=________mol/L。
(2)常温下若将0.2 mol/L MOH溶液与0.1 mol/L HCl溶液等体积混合,测得混合溶液的pH<7,则说明在相同条件下MOH的电离程度______MCl的水解程度。(填“>”、“<”或“=”)
查看答案和解析>>
科目: 来源:2013届辽宁省高二上学期期中考试化学试卷 题型:填空题
(10分)某温度(t℃)时,水的离子积为KW=1×10-13,则该温度(填“大于”、“小于”或“等于”)________25℃。若将此温度下pH=11的苛性钠溶液a L与pH=1的稀硫酸b L混合(设混合后溶液体积的微小变化忽略不计),试通过计算填写以下不同情况时两种溶液的体积比:
①若所得混合液为中性,则a∶b=________;此溶液中各种离子的浓度由大到小排列顺序是________________ 。
②若所得混合液的pH=2,则a∶b=________。此溶液中各种离子的浓度由大到小排列顺序是_______ _。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com