
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
A. -1780kJ/mol B. -1220 kJ/mol
C.-450 kJ/mol D. +430 kJ/mol
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
含11.2gKOH的稀溶液与1L0.1mol/LH2SO4溶液反应放出11.46kJ的热量,
该反应的热化学方程式正确的是。
A.KOH(aq)+1/2H2SO4(aq)=1/2K2SO4(aq)+H2O(l);△H=-11.46kJ·mol-1
B.2KOH(aq)+H2SO4(aq)=K2SO4(aq)+2H2O(l);△H=-11.46kJ·mol-1
C.2KOH+H2SO4=K2SO4+2H2O;△H=-11.46kJ·mol-1
D.KOH(aq)+ 1/2H2SO4(aq)=1/2K2SO4(aq)+H2O(l);△H=-57.3kJ·mol-1
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
为了保护地下钢管不受腐蚀,可使它与
A. 直流电源负极相连 B.铜板相连 C.锡板相连 D.直流电源正极相连
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
根据下列事实,判断离子的氧化性顺序为
①A+B2+=A2++B ②D+2H2O=D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B=B2+ +2e-
A.D2+>A2+>B2+>E2+ B.D2+>E2+>A2+>B2+
C.E2+>B2+>A2+>D2+ D.A2+>B2+>D2+>E2+
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
化学反应N2+3H2=2NH3的能量变化如图所示,E是正值,该反应的热化学方程式是
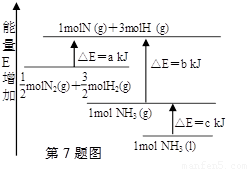
A.N2(g)+3H2(g)=2NH3(1); △H=2(a-b-c)kJ·mol-1
B. N2(g)+3H2(g)=2NH3(g); △H=2(b-a)kJ·mol-1
C.1/2N2(g)+3/2H2(g)=NH3(1); △H=(b+c-a)kJ·mol-1
D.1/2N2(g)+3/2H2(g)=NH3(g); △H=(a+b)kJ·mol-1
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s);△H=-351.1kJ·mol-1
Hg(l)+1/2O2(g)=HgO(s);△H=-90.7 kJ·mol-1,由此可知反应:
Zn(s)+HgO(s)=ZnO(s)+ Hg(l)的△H为。
A.△H=-1141.8 kJ·mol-1 B.△H=+260.4kJ·mol-1
C.△H=+441.8 kJ·mol-1 D.△H=-260.4 kJ·mol-1
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
铅蓄电池总反应为PbO2+Pb+2H2SO4═2PbSO4+2H2O,下列关于铅蓄电池的说法正确的是
A.在放电时,正极发生的反应是 Pb(s) +SO42―(aq)= PbSO4(s) +2e―
B.在放电时,该电池的负极材料是铅板
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e―= Pb(s)+ SO42―(aq)
查看答案和解析>>
科目: 来源:2013届福建省高二上学期期中考试化学试卷 题型:选择题
A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中第一电离能最大。下列有关叙述错误的是
A.四种元素A、B、C、D分别为O、Ca、Na、Ar
B.元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等
C.元素A、C简单离子的半径大小关系为A<C
D.元素B、C电负性大小关系为B>C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com