
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
甲、乙、丙、丁分别是硫酸铝、硫酸亚铁、氢氧化钠、氯化钡等四种物质中的一种,若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失。丁溶液滴入甲溶液中,无明显现象发生。据此可推断丙物质是( )
A.Al2(SO4)3 B.NaOH C.FeSO4 D.BaCl2
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是 ( )
A.铝钠合金是混合物
B.铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na)
C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出
D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
用等体积的0.1 mol·Lˉ1的BaCl2 溶液,可使相同体积的Fe2(SO4)3 、Na2SO4 、 KAl(SO4)2 三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为( )
A.3∶2∶3 B.3∶1∶2 C.2∶6∶3 D.1∶1∶1
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
下列反应的离子方程式书写正确的是 ( )
A.氯气和水的反应: C12 + H2O == 2H+ + Clˉ+ ClOˉ
B.向氯化铝溶液中加入足量氨水: Al3+ + 4NH3·H2O == AlO2- + 2H2O +4NH4+
C.用FeCl3溶液腐蚀印刷电路板: Fe3+ + Cu == Fe2+ + Cu2+
D.惰性电极电解饱和氯化钠溶液:2 Clˉ+ 2 H2O  Cl2
↑+H2 ↑+2 OHˉ
Cl2
↑+H2 ↑+2 OHˉ
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
把过氧化钠投入含有HCO3ˉ、SO32- 、NO3ˉ 、Na+ 的水溶液中,溶液中离子数目不变的是 ( )
A.HCO3- B.SO32- C.NO3- D.Na+
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moL·L-1 NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如下图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为 ( )
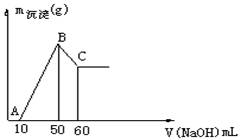
A. 1:1:1 B. 2:2:1 C. 2:1:1 D. 1:1:2
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
向Fe和Fe2O3的混合物中加入足量的稀硫酸,充分反应后生成FeSO4溶液,当生成的Fe2+和H2的物质的量之比为5︰2时,Fe和Fe2O3的物质的量之比为 ( )
A.3︰1 B.1︰2 C.2︰1 D.1∶1
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:选择题
用20mL 18.4mol·L-1 浓H2SO4与金属铜共热一段时间后,冷却,过滤,除去多余的铜,将滤液加水稀释到100mL,所得溶液中SO42-的物质的量浓度为3.18mol·L-1,则此时溶液中CuSO4的物质的量浓度为 ( )
A. 0.50 mol·L-1 B. 0.75 mol·L-1 C. 1.00 mol·L-1 D. 3.18 mol·L-1
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:填空题
(6分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应如下:
KMnO4 + HCl(浓) → KCl + MnCl2 + Cl2↑ + H2O
(1) 配平反应方程式:
KMnO4 + HCl(浓) → KCl + MnCl2 + Cl2↑ + H2O
(2)当有0.2mol电子发生转移时,生成氯气的体积(标准状况) L,被氧化的氯化氢的物质的量为 mol。该反应中HCl体现了 性和 性。
查看答案和解析>>
科目: 来源:2014届浙江省温州八校高一上学期期末考试化学试卷 题型:填空题
(共10分)请按要求回答下列问题:
(1)硅在无机非金属材料中一直扮演着重要角色,被誉为无机非金属材料的主角。
①下列物品用到硅单质的是 ;
A.玻璃制品 B.石英钟表 C.计算机芯片 D.光导纤维 E.太阳能电池
② 硅酸盐组成复杂,往往用氧化物的形式表示,某硅酸盐其主要化学成分为Ca2Mg5Si8O22(OH)2. 把它写成氧化物的形式为: ;
(2)Cl2和SO2都具有漂白性,但将这两种气体按体积比1:1通入水中得到的溶液却几乎没有漂白性,写出Cl2和SO2 1:1通入水中发生的离子反应方程式:______________________________________________________;
(3)写出二氧化硫与双氧水反应的化学方程式,并标出电子转移方向和数目: ______________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com