
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:选择题
在密闭容器中,一定量的混合气体发生反应:xA(g)+yB(g) zC(g)
zC(g)
平衡时测得A的浓度为0.50mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度降低为0.20mol/L。下列有关判断正确的是( )
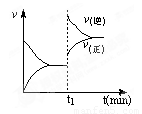
A.x+y>z
B.平衡向正反应方向移动
C.B的转化率降低
D.C的体积分数下降
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:选择题
在一定温度下的密闭容器中发生某一反应,M、N的物质的量随反应时间变化的曲线如下图,下列表述正确的是( )
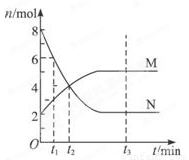
A.反应的化学方程式为2M N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:选择题
在温度压强不变时,1mol NO2高温分解,生成NO和O2,达到平衡时容器内气体的物质的量变为1.2mol,这时NO2的转化率为
A.10% B.20% C.40% D.50%
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:选择题
在一定温度不同压强(P1<P2)下,可逆反应2X(g) 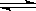 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是
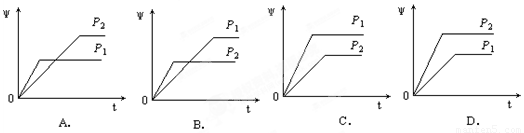
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:选择题
下图为某化学反应的速率与时间的关系示意图。在t1 时刻升高温度或增大压强,速率的变化都符合示意图的反应是 ( )
A.2SO2(g)+O2(g) ⇌ 2SO3(g);ΔH<0
B.4NH3(g)+5O2(g) ⇌ 4NO(g)+6H2O(g);ΔH<0[来源:]
C.H2(g)+I2(g) ⇌ 2HI(g); ΔH>0
D.C(s)+H2O(g) ⇌ CO(g)+H2(g);ΔH>0
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:填空题
(5分)丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2 (g) == 2H2O(l) ΔH=-d kJ·mol-1 (abcd均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________
(3)b 与a、c、d的数学关系式是______________
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:填空题
(3分)(1)在101 kPa时,1 mol CH4 完全燃烧生成CO2和液态H2O,放出890.3 kJ的热量,CH4的燃烧热为 .1120L CH4(标准状况)燃烧后所产生的热量为
(2)已知0.5 mol甲烷与0.5 mol水蒸气在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是:
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:填空题
(6分)(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ/mol,H—H键的键能是436.0 kJ/mol;由N2和H2合成1 mol NH3时可放出46.2 kJ的热量。则N—H键的键能是_______________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-24.8 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47.2 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+640.5 kJ/mol ③
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式______________________________。
(3)已知两个热化学方程式:
C(s)+O2(g)=CO2(g) △H= ― 393.5kJ/mol
2H2(g)+O2(g)=2H2O(g) △H= ― 483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是 .
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:填空题
(10分).现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则B的转化率_________。
(4) 若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______。
查看答案和解析>>
科目: 来源:2013届河南省焦作市分校高二上学期期中考试化学试卷 题型:填空题
(10分)在温度一定的条件下,向一密闭容器中加入4mol SO2 和3 mol O2,发生反应:2 SO2 (g) + O2 (g) 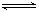 2
SO3 (g) △H<O,达到平衡后,生成了a
mol SO3。[来源:学_科_网]
2
SO3 (g) △H<O,达到平衡后,生成了a
mol SO3。[来源:学_科_网]
(1) 温度升高,该反应的化学平衡常K值___________(填增大、减小、可能增大也可能减小)。
(2)SO2的转化率为 (用字母a的表达式表示)
(3)若该反应是在恒温恒压的密闭容器中进行的。现加入8mol SO2和6mol O2 ,达到平衡后SO3气体的物质的量为 mol (用字母a表示)。如在同样的条件下,加入3mol SO2、3mol O2、x molSO3气体,达平衡后SO3在反应混合气中的体积分数与原平衡相同,则x= ,平衡后SO3的物质的量是 mol。(用含a的表达式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com