
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
下列说法正确的是( )
A.废旧电池应集中回收,并填埋处理
B.锌锰干电池工作一段时间后碳棒变细
C.太阳能电池的主要材料是高纯度的二氧化硅
D.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
用铁片与稀硫酸反应制取氢气时,下列措施不能使产生氢气的速率加快的是( )
A. 加热 B.不用稀硫酸,改用98%浓硫酸
C. 滴加少量CuSO4溶液 D. 不用铁片,改用铁粉
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
一定温度下,反应A2(g)+B2(g)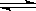 2AB(g)达到化学平衡状态的标志是(
)
2AB(g)达到化学平衡状态的标志是(
)
A.A2、B2和AB的浓度不再改变 B.A2、B2和AB在密闭容器中共存
C.容器内的压强不随时间而改变 D.单位时间里每生成1molA2,同时生成1molB2
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
对于A2
+ 3B2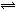 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2) =0.8mol/(L•s); B. v(A2) =0.4mol/(L•s);
C.v(C) =0.6mol/(L•s); D.v(B2) =4.2mol/(L•min)。
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子的物质的量为( )
A.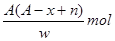 B.
B.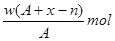
C.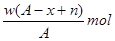 D.
D.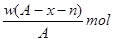
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:选择题
如图在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,两圈恰好平衡。小心地从烧杯中央滴入硫酸铜溶液。片刻后可观察到悬吊的金属圈( )
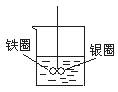
A.保持平衡状态不变 B.铁圈和银圈左右摇摆不定
C.铁圈向下倾斜 D.银圈向下倾斜
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:填空题
(13分)下表是元素周期表的一部分,回答下列有关问题:
|
周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
二 |
|
|
|
|
① |
|
② |
|
|
三 |
③ |
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
⑨ |
(1)写出下列元素符号:① ,⑦ 。
(2)画出原子的结构示意图:④ ,⑧ ;
(3)在①~⑨元素中,原子半径最大的是(除稀有气体外) ,非金属性最强的元素是 ,最不活泼的元素是 。(均填元素名称)
(4)在①~⑨元素中的氢氧化物碱性最强的是 ;元素⑥、⑦、⑧的氢化物稳定性最弱的是 (均用化学式填空)
(5)第三周期中有一种元素,其最高价氧化物的水化物具有两性,用离子方程式表示该水化物分别与稀硫酸和烧碱溶液的反应:
与稀硫酸反应: ;
与烧碱溶液反应: 。
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:填空题
(8分)某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
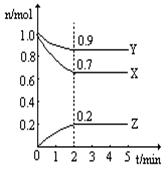
(1)该反应的化学方程式为 。
(2)反应开始至2min,以气体Z表示的平均反应速率为 。
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的 倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时____________(填“增大”“减小”或“相等”)。
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:填空题
A、B、C、D、E五种短周期元素,原子序数按A、B、C、D、E依次增大,A元素原子失去1个电子后变为质子,B元素原子的最外层电子数比次外层电子数多2个, C元素原子的最外层电子数是次外层电子数的3倍,D元素原子最外层电子数为1,E元素原子的最高价与负价的绝对值之差为4。试回答:
(1)E元素在元素周期表中的位置是
(2)由A、C二种元素共同组成的化合物中既含极性键又含非极性键的是 ,
只含极性键的是 (填化学式)。
(3)D与E可形成化合物,用电子式表示该化合物
(4)用电子式表示B、C两元素形成稳定化合物的过程
查看答案和解析>>
科目: 来源:2013届江苏省高二学业水平模拟测试化学试卷 题型:填空题
(I)将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如图所示装置。试回答下列问题:
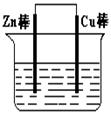
(1)若电解质溶液为稀硫酸,则Zn棒为原电池的 极,可观察到Cu棒上产生现象是 ,试用电极反应式表示该现象: 。
(2)若电解质为硫酸铜溶液,则Cu棒上发生 反应(填“氧化”“还原”),Zn棒上发生反应的电极反应式为: 。
(3)若在上述两个过程中,Zn棒减少的质量相等,则Cu棒上(1)和(2)所析出物质的质量之比为: 。
(II)A、B、C三个烧杯中分别盛有500mL相同物质的量浓度的稀硫酸
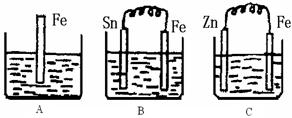
(1)写出A中离子反应方程式:
(2)一段时间后,B中Sn极附近溶液的pH (填“增大”、“减小”、“不变”)。
(3)一段时间后,C中产生了5.6L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度为
(4)反应完成后三个烧杯中液体质量大小顺序为:A B C (用<、=、>连接) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com