
科目: 来源:2013届度广东省高二第一学期期末考试化学试卷 题型:填空题
(10分)痛风是关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:①HUr(尿酸,aq) Ur-(尿酸根,aq)+H+(aq) (37℃时,Ka=4.0×10—6) ②NaUr(s)
Ur-(尿酸根,aq)+H+(aq) (37℃时,Ka=4.0×10—6) ②NaUr(s)  Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)
(1)37°时,1.0 L水中可溶解8.0×10-3mol尿酸钠,此温度下尿酸钠的Ksp为________。
(2)关节炎发作大都在脚趾和手指的关节处,这说明温度降低时,反应②的Ksp________(填“增大”、“减小”或“不变”),生成尿酸钠晶体的反应是________(填“放热”或“吸热”)反应。
(3)37℃时,某病人尿液中尿酸分子和尿酸根离子的总浓度为2.0×10-3mol·L—1,其中尿酸分子的浓度为5.0×10—4mol·L—1,该病人尿液的c(H+)为 ,PH 7(填“>”、“=”或“<”)。
查看答案和解析>>
科目: 来源:2013届度广东省高二第一学期期末考试化学试卷 题型:填空题
(14分)在一固定容积为2 L的密闭容器中加入2 molA和3 molB,保持温度为30℃,在催化剂存在的条件下进行下列反应:2A(g)+3B(g)  3C(g),2分钟达到平衡,生成1.5 mol C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol,体积分数为ω2,请回答下列问题,
3C(g),2分钟达到平衡,生成1.5 mol C,此时,平衡混合气中C的体积分数为ω1;若将温度升高到70℃后,其他条件均不变,当反应重新达到平衡时,C的物质的量为2.1 mol,体积分数为ω2,请回答下列问题,
(1) 该反应在30℃时平衡常数K1= ,焓变△H 0(填“>”、“<”或“=”)。
(2) 该反应在30℃时平衡混合气中C的体积分数为ω1= ;从反应开始到达到化学平衡状态时v(A)=____________mol/(L·min)
(3) 该反应在70℃时平衡常数为K2,则 K1 K2(填“>”、“=”或“<”)
(4) 70℃时,若保持温度不变,在2 L的密闭容器中加入4 molA和6 molB,当反应重新达到平衡时,C的体积分数为ω3,则ω3 ω2 (填“>”、“<”或“=” )。
(5) 可以判断2A(g)+3B(g)  3C(g) 反应已经达到平衡的是( )
3C(g) 反应已经达到平衡的是( )
A.2v(B)=3v(A) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.混合气体的平均相对分子质量不再改变
E.n(A)∶n(B)∶n(C)=2∶3∶3
查看答案和解析>>
科目: 来源:2013届度广东省高二第一学期期末考试化学试卷 题型:填空题
(10分)工业上冶炼钛主要以钛铁矿、金红石(含TiO2大于96%)等为原料生产。
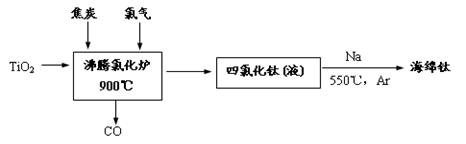
(1)由金红石为原料采用亨特(Hunter)法生产钛的流程如下:
①沸腾氯化炉中反应的化学方程式为:
②已知:Ti(s) +2Cl2(g) = TiCl4(l) △H = -804.2kJ/mol;
2Na(s) +Cl2(g) = 2NaCl(s) △H = -882.0kJ/mol
Na(s) = Na(l) △H =2.6 kJ/mol
请写出用液态钠与四氯化钛置换出钛的热化学方程式
③海绵钛破碎后用0.5%~1.5%的盐酸洗涤,再用蒸馏水洗涤至中性,用盐酸洗涤的目的是 。
(2)科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺。试回答下列有关问题。
①TiO2直接电解法(剑桥法)生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如图所示,在阴极,被还原的Ca进一步还原TiO2获得钛,则在阴极所发生的反应为: 。

②SOM技术是一种绿色环保先进技术,阳极用金属陶瓷,并用固体氧离子隔膜将两极产物隔开,只允许氧离子通过,在电解过程中阳极通入某种还原性气体,可防止CO、CO2污染物产生,通入的气体若是H2,则阳极电解反应式为 。
查看答案和解析>>
科目: 来源:2013届度广东省高二第一学期期末考试化学试卷 题型:实验题
(12分)某学生在实验室测定一未知浓度的稀盐酸,已知在25ml氢氧化钠标准溶液中逐滴加入0.2mol/L醋酸溶液的PH变化曲线如图所示:
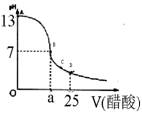
(1)该氢氧化钠溶液的物质的量浓度为 mol.L—1
(2)在B点,a 12.5ml(填“>”、“<”或“=” )。
(3)配制100 mL NaOH标准溶液所需仪器除托盘天平、玻璃棒、胶头滴管外,还需要
(4)用 量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
|
实验次数 |
第一次 |
第二次 |
第三次 |
|
消耗NaOH溶液体积/mL |
19.00 |
23.00 |
23.02 |
该盐酸的浓度约为___________________ (保留两位有效数字)。
滴定达到终点的标志是
查看答案和解析>>
科目: 来源:2012届度江西省上学期高三期末考试化学试卷 题型:选择题
随着我国经济的飞速发展,居民家用小汽车拥有量大幅攀升,汽车尾气带来的空气污染不容忽视。汽车尾气中,两种污染物能在催化剂作用下转化为无害物质,这两种污染物是( )
A、CO2和NO B、CO和NO C、CO2和O2 D、碳氢化合物和O3
查看答案和解析>>
科目: 来源:2012届度江西省上学期高三期末考试化学试卷 题型:选择题
“飘尘”是物质燃烧时产生的粒状漂浮物,颗粒很小(直径小于10-7m),不宜沉降(可漂浮数小时甚至数年),它与空气中的S02接触时,S02会转化为S03,使空气酸度增加,飘尘所起的作用与下列变化中硫酸的作用相同的是( )
A、浓硫酸与木炭共热 B、胆矾中加浓硫酸
C、乙酸乙酯与稀硫酸共热 D、浓硫酸滴到蔗糖中制“黑面包”
查看答案和解析>>
科目: 来源:2012届度江西省上学期高三期末考试化学试卷 题型:选择题
ClO2是一种消毒杀菌效率高,二次污染小的水处理剂。实验室可以通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是( )
A、KClO3在反应中失去电子 B、ClO2是氧化产物
C、1molKClO3参加反应有2mol电子转移 D、H2C2O4在反应中被氧化
查看答案和解析>>
科目: 来源:2012届度江西省上学期高三期末考试化学试卷 题型:选择题
下列与化学反应能量变化相关的叙述正确的是 ( )
A.生成物总能量一定低于反应物总能量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D. 同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H不同。
查看答案和解析>>
科目: 来源:2012届度江西省上学期高三期末考试化学试卷 题型:选择题
下列叙述错误的是 ( )
A.乙烯和苯都能使溴水褪色,褪色的原因相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com