
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
下列反应均为吸热反应,其中一定不能自发进行的是
A.(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) B.2N2O5(g)=4NO2(g)+O2(g)
C. MgCO3(s)=MgO(s)+CO2(g) D.2CO(g)=2C(s)+O2(g)
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
已知:H2(g)+F2(g) =2HF(g) △H=-270kJ∕mol,下列说法正确的是( )
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
对于反应A(g)+3B(g)  2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
A、v(A)=0.01 mol/(L•s) B、v(B)=0.02 mol/(L•s)
C、v(B)=0.60mol/(L•min) D、v(C)=1.0mol/(L•min)
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的( )
2AB2(g)△H <0,下列说法正确的( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
在密闭容器中进行下列反应:M(g)+N(g) R(g)+2L,此反应符合右边图像。下列叙述正确的是( )
R(g)+2L,此反应符合右边图像。下列叙述正确的是( )
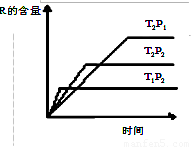
A.正反应吸热,L是气体
B.正反应吸热,L是固体
C.正反应放热,L是液体
D.正反应放热,L是气体
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
等容积的四个密闭容器中,进行同样的可逆反应:2A(g)+B(g)  3C(g)+2D(g),起始时四个容器中A、B的物质的量分别如下表所示(mol),在相同条件下建立平衡,A或B的转化率大小关系为( )
3C(g)+2D(g),起始时四个容器中A、B的物质的量分别如下表所示(mol),在相同条件下建立平衡,A或B的转化率大小关系为( )
|
|
甲 |
乙 |
丙 |
丁 |
|
A |
2 |
1 |
2 |
1 |
|
B |
1 |
1 |
2 |
2 |
A. A的转化率为:甲<丙<乙<丁 B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁 D.B的转化率为:甲>乙>丙>丁
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:选择题
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)  I3-(aq)
I3-(aq)

某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应I2(aq)+I-(aq)  I3-(aq)的ΔH>0
I3-(aq)的ΔH>0
B.若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1>K2
C.若反应进行到状态D时,一定有v正>v逆
D.状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:填空题
(14分)反应3Fe(s)+4H2O(g)= Fe3O4(s)+4H2(g),在一可变的容积的密闭容器中进行,试回答:
①增加Fe的量,其正反应速率的变化是 (填增大、不变、减小,以下相同)
②将容器的体积缩小一半,其正反应速率 ,逆反应速率 。
③保持体积不变,充入N2使体系压强增大,其正反应速率 ,逆反应速率 。
④保持压强不变,充入N2使容器的体积增大,其正反应速率 ,逆反应速率 。
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:填空题
(14分)某化学反应2A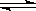 B+D在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:

根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率V(B)为 mol/(L·min)。
(2)在实验2,A的初始浓度C2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、<),且C3 1.0mol/L(填>、=、<)
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。
查看答案和解析>>
科目: 来源:2013届广东省梅州市高二上学期中考试理综试题(化学部分) 题型:填空题
(16分)
(1)1840年前后,瑞士科学家盖斯(Hess)指出,一个化学反应的热效应,仅与反应物的最初状态及生成物的最终状态有关,而与中间步骤无关,这就是著名的“盖斯定理”。现已知,在101 kPa下,CH4(g)、H2(g)、C(s)的燃烧热分别为890.3 kJ·mol-1、285.8 kJ·mol-1和393.5 kJ·mol-1,则反应C(s)+2H2(g)= CH4(g)的反应热ΔH=__________,根据以上信息,你认为“盖斯定理”在我们确定一些化学反应的反应热时有何重要意义?__________。
(2)已知:2H2(g)+O2(g)====2H2O(g) ΔH1
2H2(g)+O2(g) ====2H2O(l) ΔH2
2CO(g)+O2(g)====2CO2(g) ΔH3
①写出液态水转化为气态水的热化学方程式:___________________________________。
②CO和H2分别燃烧生成CO2(g)和H2O(g),欲得到相同热量,所需CO和H2的体积比是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com