
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
HIn(aq)
 H+(aq) + In-(aq)
H+(aq) + In-(aq)
红色 黄色
浓度为0.02 mol·L-1的下列各溶液:
①盐酸 ②石灰水 ③NaCl溶液 ④NaHSO4溶液
⑤NaHCO3溶液 ⑥氨水,
其中能使指示剂显红色的是
A.①④ B.②⑤⑥ C.①④⑤ D.②③⑥
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
等体积等物质的量浓度的NaCl和NaClO溶液,两份溶液中离子总数相比
A.前者多 B.后者多 C.一样多 D.无法判断
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
工业上制备纯硅反应的热化学方程式为:
SiCl4(g)+2H2(g)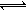 Si(s)+4HCl(g);△H = +QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
Si(s)+4HCl(g);△H = +QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是
A、反应过程中,若将硅移出体系,能提高SiCl4的转化率
B、若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C、反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(L min)
min)
D、当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好完全反应
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
分别将下列物质:①CuSO4 ②Na2O2 ③NaCl ④FeCl3 投入水中,对其溶液加热蒸干,仍能得到原物质的是
A.①②③ B.①③ C.③④ D.③
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
放热反应CO(g)+H2O(g)
 CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。其他条件不变升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol·L-1,其平衡常数为K1。其他条件不变升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
A.若增大CO浓度,K2 和K1都增大 B.K2 >K1
C.c2(CO)=c2(H2O) D.c1(CO)>c2(CO)
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是

A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:选择题
某温度下,在容积固定不变的密闭容器中发生下列可逆反应:X(g) + 2Y(g) 2Z(g)。
2Z(g)。
平衡时,X、Y、Z的物质的量分别为1 mol、1 mol、2 mol,保持温度不变,再向容器中分别充入1 mol、1 mol、2 mol的X、Y、Z,则下列叙述中正确的是
A.刚充入时,反应速率V (正)减小,V (逆)增大
B.达到新平衡时,容器内气体的平均相对分子质量增大
C.达到新平衡时,容器内气体的压强是原来的两倍
D.达到新平衡时,容器内气体的百分组成和原来相同
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:实验题
(10分)FeCl3溶液中,加入难溶于水的CaCO3粉末,观察到CaCO3逐渐溶解,产生无色气体和红褐色沉淀。则:
(1)气体为 ,红褐色沉淀为 。
(2)上述现象产生的理由是(用离子方程式及简要文字表 。
在Na2CO3溶液中滴加酚酞显红色。
(3)溶液显红色的原因是(写离子方程式) 。
(4)将溶液加热观察到的现象为 。
(5)在溶液中加足量BaCl2溶液,观察到的现象为 。
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:实验题
(7分)用中和滴定法测定某烧碱样品的纯度。(锥形瓶中装待测液)
配制待测液:将2.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制200mL溶液。
(1) 滴定:盛装0.20mol/L盐酸标准液应该用酸式滴定管;滴定时,先向盛待测液的锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视__________________________________。
滴定终点的现象是:________________ ___________________
(2) 有关数据记录如下:
|
滴定序号 |
待测液体积(ml) |
所消耗盐酸标准液的体积(ml) |
|
|
滴定前 |
滴定后 |
||
|
1 |
20.00 |
0.50 |
20.55 |
|
2 |
20.00 |
6.00 |
25.95 |
纯度计算:烧碱样品的纯度为________________。
(3) 对几种假定情况的讨论:(填无影响、偏高、偏低)(说明:测定的结果指烧碱样品的纯度)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果___________________
②若滴定前用蒸馏水冲洗酸式滴定管后即装标准盐酸,则会使测定结果__________
③滴加盐酸速度过快,未充分振荡,刚看到溶液变色,立刻停止滴定,则会使测定结果__________。
查看答案和解析>>
科目: 来源:2013届天津市高二上学期期末考试化学试卷 题型:实验题
(8分)
(1) 体积相同,pH相同的盐酸和醋酸溶液分别与足量的颗粒大小相同的锌粒反应,开始时产生氢气的速率_____________,充分反应后,产生氢气的量_____________(相同、盐酸的多、醋酸的多)
(2) 在一定量的盐酸溶液中加入足量的锌粒,若使产生氢气的量保持不变,但反应速率加快,可加入__________晶体,要使产生氢气的量不变,但反应速率减慢,可加入____________晶体。
可选择的晶体有:
(A) 纯碱 (B)烧碱 (C)胆矾 (D) 醋酸钠 (E) KHSO4
(3)某研究小组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了如下图1所示的装置。

① 在虚线框内连接合适的装置___________________

②若要比较产生气体的快慢,可以测量相同时间段内产生气体的体积,也可以测量____________________________________。
③实验测得铝丝产生气体的速率(v)与时间(t)的关系如图2所示,则t1~t2时间段内反应速率逐渐加快的主要原因是__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com