
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:选择题
可以证明恒温恒容条件下可逆反应N2 + 3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③混合气体平均相对分子质量不再改变
④体系压强不再改变
⑤NH3%、N2%、H2%都不再改变
⑥密度保持不变
⑦正反应速率v(H2) = 0.6mol/(L·min),逆反应速率v(NH3) = 0.4mol/(L·min)
A.全部 B.只有①③④⑤ C.②③④⑤⑦ D.只有③⑤⑥⑦
查看答案和解析>>
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:实验题
Ⅰ.下列有关实验操作或结果的说法中正确的是 (填字母)
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.用碱式滴定管量取0.10 mol·L-1的KMnO4溶液15.10 mL
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
G.测定酸碱滴定曲线:开始时测试和记录的间隔可稍小些,滴定至终点附近则要大些
Ⅱ.(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式 。已知H2O(l) = H2O(g) ΔH =+44 kJ·mol-1 则标准状况下33.6 L H2 生成液态水时放出的热量是 kJ。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量。已知白磷P4和P4O6的分子结构如下图所示:
现提供以下化学键的键能:P-P 198 kJ·mol-1 P-O 360 kJ·mol-1,氧气分子内氧原子间的(O=O)键能为498 kJ·mol-1。则P4+3O2 = P4O6的反应热ΔH为 。
查看答案和解析>>
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:填空题
有浓度均为0.1 mol•L-1的盐酸、硫酸、醋酸三种溶液,试回答:
(1) 三种溶液中c(H+) 依次为a mol•L-1,b mol•L-1,c mol•L-1,其大小顺序为_____。
(2)等体积的以上三种酸分别与过量的NaOH 溶液反应,生成的盐的物质的量
依次为n 1mol,n2 mol,n3 mol,它们的大小关系为____________ 。
(3)中和一定量NaOH溶液生成正盐时,需上述三种酸的体积依次是V1L、V2L、V3L,其大小顺序为____________ 。
(4)等体积的上述三种酸与足量的锌反应,产生氢气的体积(相同条件下)分别为V1L、V2L、V3L,其大小顺序为____________ 。
查看答案和解析>>
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:填空题
某同学用中和滴定法测定某烧碱样品的纯度,其操作步骤如下:
①称取25.0g烧碱样品,配成1L溶液;
②用 (填仪器名称)量取10.00mL配制好的溶液于锥形瓶中,用0.20mol·L-1的标准盐酸滴定(杂质不与盐酸反应),所得数据如下表,其中第2组数据读数如图所示。
|
滴定序 号 |
待测液体积/mL |
所消耗盐酸标准液的体积/mL |
||
|
滴定前 |
滴定后 |
消耗的体积 |
||
|
1 |
V |
0.50 |
25.52 |
25.02 |
|
2 |
V |
|
|
|
|
3 |
V |
1.00 |
25.98 |
24.98 |
请回答下列问题:
(1)根据滴定管的读数填写上表。
(2)实验过程中,配制溶液定容时俯视刻度线会使所配溶液浓度 (填“偏大”“偏小”或“无影响”,下同);滴定前仰视液面,滴定后平视液面会使烧碱样品纯度的测量值比实际值 。
(3)三组数据中,因误差过大而应舍去的一组是第 组(填序号),根据合理数据求得该烧碱样品中NaOH的质量分数为 。
查看答案和解析>>
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:填空题
在溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为
C分别在三种不同实验条件下进行,它们的起始浓度均为 、
、 及
及 。反应物A的浓度随时间的变化如下图所示。
。反应物A的浓度随时间的变化如下图所示。

请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②____________ ;
③_______________ ;
(2)实验②平衡时B的转化率为________;实验③平衡时C的浓度为__________;
(3)该反应的 _______0,判断其理由是________________________________;
_______0,判断其理由是________________________________;
(4)该反应进行到4.0min时的平均反应速率:
实验②: =_______________________;实验③:
=_______________________;实验③: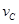 =____________________。
=____________________。
查看答案和解析>>
科目: 来源:2010年黑龙江牡丹江一中高二上学期期中考试化学试卷 题型:填空题
一定温度下,将2mol A和2mol B两种气体混合于体积为2 L的某恒容的密闭容器中,发生如下反应:3A(g)+B(g) x
C(g)+2D(g),
x
C(g)+2D(g), H <0,2min 末反应达到平衡状态(温度不变),生成了0.8 mol D,并测得C的浓度为0.4
mol/L,请填写下列空白:
H <0,2min 末反应达到平衡状态(温度不变),生成了0.8 mol D,并测得C的浓度为0.4
mol/L,请填写下列空白:
(1)X的值等于 ,
(2)该反应的化学平衡常数K= ,升高温度时K值将
(填“增大”、“减小”、“不变”)
(3)A物质的转化率为 。
(4)若维持温度不变,在原平衡混合物的容器中再充入3mol C和3mol D,欲使达到新的平衡时,各物质的物质的量分数与原平衡相同,则至少应再充入B的物质的量为 mol;达新平衡时,A的物质的量为n(A)= mol。
查看答案和解析>>
科目: 来源:2010年黑龙江省五大连池市等五校联谊高一下学期期末考试 题型:选择题
下列变化中,属于物理变化的是:( )



A.煤的干馏 B.石油的分馏 C.石油的裂化 D.铝热反应
查看答案和解析>>
科目: 来源:2010年黑龙江省五大连池市等五校联谊高一下学期期末考试 题型:选择题
某元素原子核内质子数为m,中子数为n,则下列论断正确的是( )
A.不能由此确定该元素的原子量 B.这种元素的原子量为m+n
C.若碳原子质量为ωg,此原子的质量为(m+n)ω
D.核内中子的总质量小于质子的总质量
查看答案和解析>>
科目: 来源:2010年黑龙江省五大连池市等五校联谊高一下学期期末考试 题型:选择题
下列物质中既含有离子键又含有非极性共价键的是( )
A.NaOH B.Na2O2 C.CaCl2 D.H2O2
查看答案和解析>>
科目: 来源:2010年黑龙江省五大连池市等五校联谊高一下学期期末考试 题型:选择题
下列化学用语的书写正确的是
A.乙酸的分子式:C2H4O2 B.乙醇的结构简式:C2H6O
C.F原子结构示意图: D.四氯化碳的电子式:
D.四氯化碳的电子式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com