
科目: 来源:2010年福建省、长汀一中高二下学期期末联考化学试题 题型:填空题
(12分)固定和利用CO2能有效地利用资源,并减少空气中的温室气体.CO2与化合物A反应生成化合物B,如下反应式(其它试剂、产物及反应条件均省略)。

(1)化合物B的分子式为__________,1 mol该物质完全燃烧需消耗_________mol O2 。
(2)由 通过消去反应制备A的化学方程式为(注明反应条件):
通过消去反应制备A的化学方程式为(注明反应条件):
_______________________________________________________________________。
(3)B与过量C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为:
__________________________________________。
(4)与CO2类似,CO也能被固定和利用。在一定条件下,CO、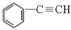 和
和
H2三者发生反应(苯环不参与反应),生成化合物C的分子式为C9H8O,且物质C能发生银镜反应。写出生成物C可能的结构简式:
___________________________________________________________________。
查看答案和解析>>
科目: 来源:2010年福建省、长汀一中高二下学期期末联考化学试题 题型:填空题
(12分)在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K=__________________________。
已知:K(300℃)>K(350℃),该反应是__________热反应(填“放”或“吸”)。
(2)上述反应达平衡时,NO的转化率=__________________。
(3)下图中表示NO2的变化的曲线是____________(选填字母,下同)。

(4)能说明该反应已经达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.NO和NO2两物质的浓度相等
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂
查看答案和解析>>
科目: 来源:2010年福建省、长汀一中高二下学期期末联考化学试题 题型:填空题
(10分)W、X、Y、Z是短周期主族元素,它们的核电荷数依次增大。下表列出它们的性质和原子结构:
|
元素编号 |
元素性质或原子结构 |
|
W |
原子电子层数与核外电子数相等 |
|
X |
核外s能级上的电子总数与p能级上的电子总数相等 |
|
Y |
元素的原子半径在该周期中最大(除稀有气体外) |
|
Z |
原子核外p能级上的电子总数比s能级上的电子总数多2[来源:Zxxk.Com] |
(1)元素符号:X_______________,Z________________。
(2)Y元素原子的核外电子排布式为__________________。
(3)X元素原子的核外有 种不同形状的电子云。
(4)Y元素的单质在W和X形成的化合物中反应的离子方程式为
___________________________________________________________________ 。
查看答案和解析>>
科目: 来源:2010年福建省、长汀一中高二下学期期末联考化学试题 题型:填空题
(12分)
(1)在250C、101KPa时,1g甲醇完全燃烧生成CO2和液态水时放热22.68kJ,则能表示甲醇燃烧的热化学方程式为:
________________________________________________________________________。
(2)已知:C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:
C(s)+O2(g)=== CO2(g); △H=—394kJ·mol—1;
2CO(g)+O2(g)=== 2CO2(g); △H=—566kJ·mol—1;
2H2(g)+O2(g)=== 2H2O(g); △H=—484 kJ·mol—1;
①在25℃、101KPa时,1 g 甲醇不完全燃烧生成1∶1的CO、CO2和液态水,写出此甲醇燃烧的热化学方程式:
_____________________________________________________________________。
②工业上可由CO和H2合成甲醇。试写出由C(s)与水蒸气在高温条件下反应生成氢气
和一氧化碳的热化学方程式 。
(3)利用甲醇可设计燃料电池。
①如用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入甲醇和氧
气。写出负极的电极反应式 。
②下列有关甲醇燃料电池的说法中,错误的是_________
A.甲醇燃料电池的负极发生氧化反应
B.甲醇燃料电池的电子由负极、经外电路流入正极
C.甲醇燃料电池在负极区产生CO
D.甲醇燃料电池中使用的氢氧化钾浓度保持不变
查看答案和解析>>
科目: 来源:2010年福建省高一第二学期半期考试化学试题 题型:选择题
19世纪中叶,俄国化学家门捷列夫的突出贡献是 ( )
A.提出原子学说 B.发现元素周期律 C.提出分子学说 D.发现氧气
查看答案和解析>>
科目: 来源:2010年福建省高一第二学期半期考试化学试题 题型:选择题
在元素周期表中,第3、4、5、6周期所含元素的数目分别是 ( )
A.8、18、32、32 B.8、18、18、32
C.8、18、18、18 D.8、8、18、18
查看答案和解析>>
科目: 来源:2010年福建省高一第二学期半期考试化学试题 题型:选择题
根据原子序数推断,下列各组元素化合时能以离子键结合的是 ( )
A.10与19 B.6与16 C.11与17 D.14与8
查看答案和解析>>
科目: 来源:2010年福建省高一第二学期半期考试化学试题 题型:选择题
某元素最高价氧化物对应水化物的分子式是H4RO4,则其氢化物的分子式( )
A.RH4 B.RH3 C.H2R D.HR
查看答案和解析>>
科目: 来源:2010年福建省高一第二学期半期考试化学试题 题型:选择题
某微粒用 AZQn+表示,下列关于该微粒的叙述正确的是( )
A.所含质子数= A-n B.所含中子数=A-Z
C.所含电子数=Z+n D.质量数=Z+A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com