
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
在下列各组离子在一定条件下能够大量共存的是
A.无色溶液:Cu2+、K+、MnO4-、SO42-
B.能溶解Al2O3的溶液:Na+、Ca2+、HCO3-、NO3-
C.c(OH-)=1×10-13mol·L-1的溶液:NH4+、Al3+、SO42-、Cl-
D.含0.1 mol·L-1 NO3-的溶液:H+、Fe2+、Mg2+、Br-
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
A、B、C、D、E、F为原子序数依次增大的短周期元素,其中A与E同主族,B与F同主族,E与F同周期,已知常温下A、E单质的状态不同,D原子的核电荷数是B原子最外层电子数的2倍,F单质是一种重要的半导体材料。下列说法正确的是
A.原子半径由大到小的顺序是:
B.由A、C、D三种元素组成的化合物中可能含有离子键
C.F、C、B元素最高价氧化物对应的水化物的酸性依次增强
D.F与D形成的化合物质地坚硬,既不与酸反应也不与碱反应
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
25℃时,下列溶液中微粒的物质的量浓度关系正确的是

A. 的
的 与
与 混合溶液中:
混合溶液中: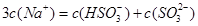
B.0.1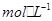 的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
的KHA溶液,其PH=10 c(K+)﹥c(OH-)﹥c(HA-)
C.20mL
0.1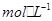 醋酸钠溶液与10mL 0.1
醋酸钠溶液与10mL 0.1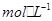 盐酸混合后的溶液中:
盐酸混合后的溶液中:
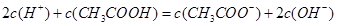
D.在25mL
0.1 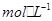
 溶液中逐滴加入0.2
溶液中逐滴加入0.2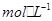
 溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:
溶液,溶液pH变化如右图所示,在A、B间任一点,溶液中一定都存在下列关系:

查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
向100 g FeCl3溶液中放入一小块钠,待反应完全后,过滤,得到仍有棕黄色的溶液91.8g,则投入钠的质量为
A.18.4g B.13.8g C.8.2g D.9.2g
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是

|
选项 |
X |
Y |
Z |
甲 |
乙 |
|
A |
H2 |
Si |
C12 |
SiCl4 |
HCl |
|
B |
Mg |
C |
O2 |
CO2 |
MgO |
|
C |
Zn |
Fe |
Cl2 |
FeCl2 |
ZnCl2 |
|
D |
O2 |
N2 |
H2 |
NH3 |
H2O |
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
一定条件下,在体积为10 L的密闭容器中,2 mol A和2
mol B 进行反应:2A(g) +B(g)  C(g),经60s达到平衡,生成0.6 mol C。下列说法正确的是
C(g),经60s达到平衡,生成0.6 mol C。下列说法正确的是
A.以A浓度变化表示的反应速率为0.002 mol·(L·s)-1
B.若增大压强,则物质B 的转化率减小
C.若升高温度,A的体积分数增大,则该反应的△H>0
D.将容器体积变为20 L,C的平衡浓度变为原来的1/2
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
下列排列顺序正确的一组是 ( )
A.粒子半径:Fe(OH)3胶粒>I->Na+>F- B.氧化性:MnO >Fe3+>Cu2+>Zn2+
>Fe3+>Cu2+>Zn2+
C.酸性:H3PO4<H2CO3<H2SiO4<H2SO4 D.热稳定性: NaHCO3<Na2CO3<CaCO3<Al2O3
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:选择题
接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是( )
①尾气用氨水处理 ②污水用石灰乳处理
③废渣用来造水泥、炼铁 ④设置“废热”锅炉产生蒸汽,供热或发电。
A.只有①② B.只有①③④ C.只有①②③ D.全部
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:实验题
近期因“召回门”而闹的沸沸扬扬的丰田Prius属第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态。

(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为_________________________________。
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液。镍氢电池充放电原理示意如图,其总反应式是:
根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将_______(填“增大”、“不变”或“减小”),该电极的电极反应式为_________________。
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:
CO(g)+1/2O2(g)  CO2(g)。一定温度下达平衡时
CO2(g)。一定温度下达平衡时 是一个常数。
是一个常数。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请填写表中的空格。
|
容器编号 |
c(CO)/mol·L-1 |
c (O2)/mol·L-1 |
c (CO2)/mol·L-1 |
v(正)和v (逆) 比较 |
|
I |
2.0×10-4 |
4.0×10-4 |
4.0×10-2 |
v(正)=v(逆) |
|
Ⅱ |
3.0×10-4 |
4.0×10-4 |
5.0×10-2 |
|
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol·L-1和1.0×10-4mol·L-1。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol·L-1,则最终尾气中CO的浓度为_________mol·L-1。
查看答案和解析>>
科目: 来源:2010年河北正定中学高三年级第四次考试 题型:实验题
锂被誉为“高能金属”。工业上用硫酸与β-锂辉矿(LiAlSi2O6和少量钙镁杂质)在250~300℃反应,生成Li2SO4以及硅铝化合物、MgSO4等,其工业生产流程如下:

(1)用氧化物形式表示LiAlSi2O6的组成:___________________。
(2)沉淀X的主要成分是(写化学式)________________________。
(3)流程中两次使用了Na2CO3溶液,试说明前后浓度不同的原因:
____________________________________________________________________。
(4)锂和氢气在加热时能反应生成白色固体氢化锂,氢化锂遇到水就立即溶解并释放出大量的气体。试写出氢化锂遇水反应的化学方程式:_____________________________________。
(5)将盐酸与Li2C03完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com