
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
下列说法不正确的是( )
A.有固体Mg(OH)2存在的饱和溶液中加入NH4Cl固体,能使Mg(OH)2固体减少
B.为了避免电解液中CuSO4因水解发生沉淀,可加入适量稀硫酸抑制水解
C.在蒸发皿中加热蒸干碳酸钠的溶液,可以得到碳酸钠固体
D.溶液导电过程是电解的过程,强电解质溶液的导电能力一定比弱电解质溶液强
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
已知铅蓄电池的总反应PbO2 +Pb +2H2SO4== 2PbSO4 + 2H2O ,图为铁铆钉铆在铜板上,有关叙述不正确的是

A.铅蓄电池放电时,电路中每转移2mol电子,消耗1mol硫酸
B.铅蓄电池充电时,阳极电极反应为PbSO4 + 2H2O- 2e- == PbO2 + 4H+ + SO42-
C.铅蓄电池放电时,内电路硫酸根离子向铅极移动, 正极附近溶液的pH增大
D.如图,铁铆钉发生吸氧腐蚀,在铁钉附近滴加K3[Fe(CN)6]溶液,可观察铁钉附近有蓝色沉淀产生
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
下列描述中正确的是( )
A.电解法制镁时一般是用熔融态的氯化镁进行电解,但也可用氯化镁溶液
B.电解法生产铝时,可用钢网代替碳棒作阳极增大接触面积
C.我国第五套人民币中的一元硬币材料为钢芯镀镍,在硬币制作时,钢芯应做阴极
D.用电解法制备高纯度的镍,粗镍做阴极,精镍作阳极,阳极质量的减少与阴极质量的增加相等
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
下列液体均处于25℃,有关叙述正确的是
A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐
B.pH=4的NH4Cl溶液,溶液中c (H+)>c (OH-),且c (H+)/c (OH-)=1×106
C.AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
D.冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
工业制硝酸的其中一步反应为氨的氧化,反应方程式为:
4NH3(g)+ 5O2(g) 4NO(g)+ 6H2O(g) △H< 0。有关该反应的说法正确的是
4NO(g)+ 6H2O(g) △H< 0。有关该反应的说法正确的是
A.反应达到平衡后,3ν正(NH3)=2ν逆(H2O)
B.反应处于平衡状态时,c(NH3)·c(O2)=c(NO)·c(H2O)
C.其它条件不变,温度越高,氨的转化率越高
D.增大压强是加快反应速率并提高NO产率的有效措施
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
某温度下,在容积固定不变的密闭容器中发生下列可逆反应:
2X(g) + Y(g)  2Z(g) △H =-Q kJ/mol平衡时,X、Y、Z的物质的量分别为1 mol、1 mol、2
mol,放出热量Q kJ,保持温度不变,再向容器中分别充入1 mol、1 mol、2 mol的X、Y、Z,则下列叙述中正确的是
2Z(g) △H =-Q kJ/mol平衡时,X、Y、Z的物质的量分别为1 mol、1 mol、2
mol,放出热量Q kJ,保持温度不变,再向容器中分别充入1 mol、1 mol、2 mol的X、Y、Z,则下列叙述中正确的是
A.原平衡时,X的转化率为50%
B.达到新平衡时,X的转化率不变
C.达到新平衡时,容器内气体的平均相对分子质量增大
D.达到新平衡时,平衡常数K增大
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
常温下,①PH=10氨水 ②PH=10氢氧化钠溶液 ③PH=4 HA溶液 ④PH=4 HB溶液,对下列四种溶液的叙述正确的是
A.②、④两溶液相比,两者的kw相同,水的电离程度不相同
B.若酸性HA比HB的强,则等物质的量浓度的NaA、NaB溶液PH:NaA>NaB
C.一定体积①、10mL③ 两溶液混合,PH=7,V总≥20mL
D.等体积的②,分别用③、④中和,消耗酸溶液的体积V③ > V④,则说明HA的酸性比HB的酸性强
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是
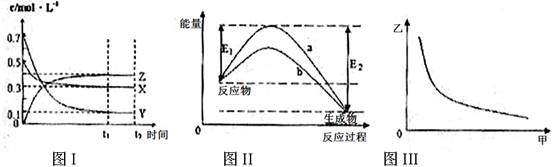
A.该反应热化学方程式为X(g) +3Y(g)  2Z(g) △H= —(E2―E1)
2Z(g) △H= —(E2―E1)
B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线
C.若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a一定是没有加入催化剂时的能量变化曲线
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
控制适合的条件,将反应Fe2++Ag+  Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是
Ag + Fe3+设计成如下图所示的原电池。下列判断错误的是

A.反应开始时,电子从甲中石墨经导线流向乙中石墨
B.电流计指针为零时,上述反应的正反应速率等于逆反应速率
C.电流计读数为零后,在甲中加入FeCl3固体,乙中石墨电极反应为Ag - e- == Ag+
D.电流计读数为零后,在乙中加入硫化钠固体,电流计指针读数仍为零
查看答案和解析>>
科目: 来源:2010年北京市高二第二学期期末考试化学试卷 题型:选择题
如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始VA=VB= aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应:
X(g)+Y(g) 2Z(g)+W(g) △H>0;达到平衡时,VA=1.2aL,则下列说法错误的是
2Z(g)+W(g) △H>0;达到平衡时,VA=1.2aL,则下列说法错误的是

①反应开始时,B容器中化学反应速率快
② A容器中X的转化率为40%,且比B容器中X的转化率大
③打开K达新平衡后,升高B容器温度,A容器体积会增大
④打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
A.①②③④ B.①②③ C.② ④ D.只有④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com