
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都是正确的是:
A.黄铁矿煅烧前需要粉碎,因为大块的黄铁矿不能在空气中反应[来源:ZXXK]
B.从沸腾炉出来的炉气需净化,因为炉气中二氧化硫会与杂质反应
C.二氧化硫氧化为三氧化硫时需使用催化剂,这样可以提高二氧化硫的转化率
D.三氧化硫用98.3%的浓硫酸吸收,目的是防止形成酸雾,以提高三氧化硫的吸收效率
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
下列说法或表示方法正确的是
A.若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由“C(石墨)=C(金刚石) ΔH=1.9kJ/mol”可知,金刚石比石墨稳定
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=285.8kJ/mol
D.在稀溶液中:H++OH-=H2O ΔH=-57.3kJ/mol,若将含1molCH3COOH与含1mol NaOH的溶液混合,放出的热量小于57.3kJ
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
中学化学教材中有大量数据,下列为某同学对数据的利用情况,其中不正确的是:
A. 用溶解度数据判断煮沸Mg(HCO3)2溶液得到的产物是Mg(OH)2而不是MgCO3 。
B. 用pH数据推测不同强酸弱碱盐在水溶液中水解程度的大小。
C. 用反应热数据的大小判断不同反应的反应速率的快慢。
D. 用平衡常数的大小判断化学反应可能进行的程度。
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
对于工业制硫酸中接触室内的反应:2SO2(g)+O2 (g)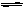 2SO3(g) △H<0 。达到平衡时,只改变下列一个条件,平衡不发生移动的是:
2SO3(g) △H<0 。达到平衡时,只改变下列一个条件,平衡不发生移动的是:
A. 升高温度 B. 恒温、恒容充入氧气
C. 恒温恒容充入SO3 D. 加入催化剂V2O5
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
某温度下,对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(P)的关系如图所示。下列说法正确的是:

A. 将1.0mol氮气、3.0mol氢气,置于1L密闭容器中发生反应,放出的热量为92.4kJ。
B. 平衡状态由A变到B时,平衡常数K(A) < K(B) 。
C. 上述反应在达到平衡后,增大压强,H2的转化率提高。
D. 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小。
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
其他条件不变的情况下,下列说法不正确的是:
A. 对于反应nA(g)+B (g)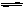 2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
2C(g),平衡后增大压强,A的百分含量减小,则n≥2。
B. 对于反应2A(g)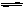 B(g) △H<0,若体系温度不再变化说明反应达到平衡状态。
B(g) △H<0,若体系温度不再变化说明反应达到平衡状态。
C. 对于反应2A(g)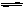 B(g),恒温、恒容条件下气体密度不再变化说明反应达到平衡状态。
B(g),恒温、恒容条件下气体密度不再变化说明反应达到平衡状态。
D. 对于反应2A(g)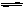 B(g),若ν(A)正=2ν(B)逆,说明反应达到平衡状态。
B(g),若ν(A)正=2ν(B)逆,说明反应达到平衡状态。
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600℃~700℃,所用燃料为H2,电解质为熔融的K2CO3。该电池的总反应为:2H2+O2
2H2O,负极反应为:H2+CO32-→H2O+CO2+2e-。则下列推断中,正确的是( )
A.正极反应为4OH—→2H2O+O2↑+4e- B.当电池生成1mol水时,转移4mol电子
C.放电时CO32-向负极移动 D.通H2的一极为负极,发生还原反应
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是:

A.从E口逸出的气体是H2
B.从B口加入含少量NaOH的水溶液以增强导电性
C.标准状况下每生成22.4 L Cl2,便产生2 mol NaOH
D.粗盐水中含Ca2+、Mg2+、Fe3+、SO等离子,精制时先加Na2CO3溶液
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应为: 。下列说法不正确的是:
。下列说法不正确的是:
A.放电时,负极的电极反应式:Li-e-=Li+
B.放电和充电过程恰好相反,则充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
查看答案和解析>>
科目: 来源:2012届济南市高二第二学期期末考试化学试卷(理科) 题型:填空题
下列说法正确的是:
A.95℃时纯水的pH<7,说明加热可以使纯水呈酸性。
B.25℃时,pH=12的某溶液中,由水电离出的c(OH-)一定为1×10-12mol/L。
C.pH=3的醋酸溶液,稀释至10倍后pH=4。
D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配制FeCl3溶液。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com