
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
有下列三个反应:①Cl2 + FeI2 = FeCl2 + I2 ②2Fe2+ + Br2 = 2Fe3+ + 2Br-
③Co2O3 + 6HCl = 2CoCl2 + Cl2↑+ 3H2O ,下列说法正确的是 ( )
A.①②③中的氧化产物分别是FeCl2 、Fe3+、Cl2
B.根据以上方程式可以得到氧化性Cl2 > Co2O3 > Fe3+
C.在反应③中生成1mol Cl2时,有2molHCl被氧化
D.根据反应①②一定可以推理得到Cl2 + FeBr2 = FeCl2 +Br2
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
定温度、压强和有铁触媒的条件下,在密闭容器中充入N2、H2和NH3 。若起始时n(N2)=x mol、n(H2)=y mol、n(NH3)=z mol (x、y、z均不为0 ),平衡时,n(N2)=0.1mol、n(H2)=0.3mol、n(NH3)=0.08mol。下列有关判断不合理的是 ( )
A.x : y =1 : 3
B.N2、H2的转化率不相等
C.平衡时,H2与NH3的生成速率之比为3 : 2
D.x的取值范围为0<x<0.14
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
在一密闭容器中有如下反应:L (s) + a G (g) 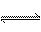 b
R (g)
b
R (g)
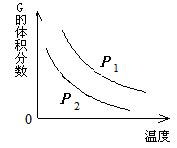 温度和压强对该反应的影响如右图所示,其中压强P1 <
P2,
温度和压强对该反应的影响如右图所示,其中压强P1 <
P2,
由此可判断 ( )
A. 正反应为放热反应
B. 化学方程式中的计量数a > b
C. G的转化率随温度升高而减小
D. 增大压强,容器内气体质量不变
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
 已知反应2SO2(g)+O2(g)
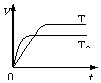
已知反应2SO2(g)+O2(g) 2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是 (
)
2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是 (
)
A.O2的体积分数
B.混合气体的密度
C.密闭容器内的压强
D.SO2的转化率
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
某温度下反应N2O4(g) 2NO2
(g);ΔH>0,在密闭容器中达平衡,下列说法正确的是 ( )
2NO2
(g);ΔH>0,在密闭容器中达平衡,下列说法正确的是 ( )
A.保持体积不变,加入少许N2O4,平衡向逆反应方向移动
B.升高温度v正、v逆都增大,v正增大的倍数小于v逆增大的倍数
C.保持体积不变,升高温度,再达平衡时混和气体颜色变深
D.达到平衡后,降低温度或减小压强平衡移动的方向一致
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O (g) ;△H=―574 kJ·mol-1
② CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g);△H=―1160 kJ·mol一1。
下列选项正确的是 ( )
A.CH4(g)+2NO2(g)= N2 (g)+CO2(g)+2H2O (l);△H=―867 kJ·mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为1.6 mol
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:单选题
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是 ( )
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:填空题
(12分)合成氨生产技术的创立开辟了人工固氮的途径,对化学工业技术也产生了重大影响。合成氨反应的化学方程式为:N2(g)+3H2(g) 2NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题:
2NH3(g) ,△H=-92.2kJ/mol。合成氨工业中原料气N2可从空气中分离得到,H2可用甲烷在高温下与水蒸气反应制得。我国合成氨工业目前的生产条件为:催化剂-铁触媒,温度-400~500℃,压强-30~50MPa。回答下列问题:
(1)合成氨工业中原料气压缩到30~50MPa的原因是 。从平
衡移动原理分析,低温有利于原料气的转化,实际生产中采用400~500℃的高温,
原因之一是考虑到催化剂的催化活性,原因之二是 。
(2)500℃、50MPa时,在容积为VL的容器中加入n mol N2、3n mol H2,反应达平衡后
测得平衡常数为K1,此时N2的转化率为x。则K1和x的关系满足K1= 。
若温度为400℃,平衡常数为K2,则K1 K2(填“<”、“=”或“>” )
(3)甲烷在高温下与水蒸气反应的热化学反应方程式为:
CH4(g)+H2O(g)=CO(g)+3H2(g);△H kJ·mol-1。
又已知: H2(g) +1/2 O2(g)== H2O(l);△H1=-285.8kJ/mol
CO(g) + 1/2 O2(g)=CO2(g);△H2=-283.0kJ/mol
CH4(g) +2 O2(g)== CO2(g)+ 2H2O(l);△H3=-890.3kJ/mol
H2O(g)== H2O(l); △H4=-44.0kJ/mol
①写出H2(g)完全燃烧生成气态水的热化学方程式 。
②CH4(g)+H2O(g)=CO(g)+3H2(g); △H= kJ/mol
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:填空题
(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
 +4H++3e-====NO+2H2O
。 已知Cu2O能使上述还原过程发生。
+4H++3e-====NO+2H2O
。 已知Cu2O能使上述还原过程发生。
(1)写出并配平该氧化还原反应的化学方程式:______________。
(2)反应中硝酸体现了________、_________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是___________mol。
(4)若1 molCu2O与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是_______。
查看答案和解析>>
科目: 来源:福建省厦门外国语学校2010-2011学年高三第一次月考 题型:填空题
(8分)微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体,将有机物的化学能转化为电能。以葡萄糖溶液作底物为例,其工作原理如右图所示。

 已知石墨电极上反应为:
已知石墨电极上反应为:
C6H12O6+6H2O-24e- 6CO2+24H+
(1)电池中的质子交换膜只允许质子和水分子通过。
电池工作时,质子移向电源的 极,
铂碳上所发生的电极反应式为_____________。
(2)燃烧热是指1摩尔物质完全燃烧生成稳定的物质(如H转化为液态水,C转化为二氧化碳 )所放出的热量。葡萄糖的燃烧热为2800kJ/mol,写出葡萄糖燃烧的热化学方程式 。
(3)化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是 (填序号)。
|
序号 |
A |
B |
C |
D |
E |
|
污水类型 |
生活污水 |
印染 |
电镀 |
造纸 |
硫酸工业废水 |
|
COD值(mg/L) |
520 |
870 |
20 |
960 |
120 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com