
科目: 来源: 题型:022
在某些条件下,容器中有如下平衡反应:A + 4B![]() 2C + D + Q此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
2C + D + Q此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
(1)改变a的取值,再通过改变反应条件,可以使反应重新达到平衡。并限定达到新的平衡时,D的物质的量只允许在![]() 到2d之间变化,则a的取值范围应是____________(用a和d的关系式表示)。
到2d之间变化,则a的取值范围应是____________(用a和d的关系式表示)。
(2)如果要使本反应重新建立的平衡中,D的物质的量只允许在d到2d之间取值,则应该采取的措施是( )
A.升高反应温度
B.增大反应容器内压强
C.增大反应容器容积
D.降低反应温度
E.减小反应容器内压强
F.减小反应容器容积
查看答案和解析>>
科目: 来源: 题型:022
下列物质:①N2 ②NH4Cl ③NaCl ④KOH ⑤NH3 ⑥CaC2
(1)固态时属于离子晶体的有_________(填序号,下同);
(2)受热熔化时只破坏离子键的有________;
(3)含共价键的离子晶体有________;
(4)溶于水时只破坏离子键的有________。
查看答案和解析>>
科目: 来源: 题型:022
分别把KCl和NaNO3晶体溶于盛有适量水的同一烧杯内,再将溶液蒸发至全部晶体析出,则析出的晶体最多可能是________种物质,它们的化学式分别是________。
查看答案和解析>>
科目: 来源: 题型:022
发射航天器的火箭可用肼作燃料,肼又叫联氨,其化学式为(NH2)2,为无色可燃性液体,熔点275 K,沸点386.5 K。1 g肼燃烧时放出19.5 kJ的热量(通常状况下测定),是一种清洁的能源物质。古典的Rasching法制备肼是以次氯酸钠和足量的氨反应,获得肼的稀溶液,经分析确定该溶液中含有氯离子。回答下列问题:
(1)写出肼的电子式__________。
(2)古典Resching法制备肼的化学方程式:______________________。
(3)肼燃烧的热化学方程式:_____________________。
查看答案和解析>>
科目: 来源: 题型:022
长征二号火箭的主要燃料是我叫“偏二甲肼”的液体物质。此化合物的相对分子质量为60。其中,含碳的质量分数为40%,氢的质量分数为13.33%,其余为氮。则:
(1)偏二甲肼的化学式为_______,若该分子中的氮原子均以![]() 的形式存在,且其中
的形式存在,且其中![]() 一个氮原子不与氢原子直接相连,则偏二甲肼的结构简式为_________。
一个氮原子不与氢原子直接相连,则偏二甲肼的结构简式为_________。
(2)此燃料的氧化剂是N2O4气体,若燃烧0.2 mol偏二甲肼液体放出的热量为a kJ(a>0),燃烧的产物只有N2、CO2、H2O(均为气态),则偏二甲肼燃烧的热化方程式为_____________________。
(3)火箭起发时,一级火箭中部冒出红棕色气体,这是排出的部分氧化剂变化而来,其化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:022
已知下列变化过程中,有0.2 mol RxO![]() 参加反应,转移0.4 mol电子。
参加反应,转移0.4 mol电子。
□RxO![]() +□MnO
+□MnO![]() +□ H+——□RO
+□ H+——□RO![]() +□Mn2++□H
+□Mn2++□H![]() O
O
(1)推算出x值为___________;
(2)配平该离子方程式;
(3)反应中还原剂为___________;
(4)在上述变化过程中,参加反应的H+的物质的量为______mol。
查看答案和解析>>
科目: 来源: 题型:022
某化工厂用NH3制备NH4NO3。已知由NH3制NO的产率是96%,NO制HNO3的产率是92%,HNO3与NH3反应生成NH4NO3,则制HNO3所用去的NH3的质量占总耗NH3质量的_ %(不计生产上的其他损耗)。
查看答案和解析>>
科目: 来源: 题型:022
硝酸工业尾气中的氮的氧化物(NO、NO2)是主要的大气污染物之一,其常用的治理方法有以下几种:
①NaOH溶液吸收法,反应原理如下:
2NO2+2NaOH====NaNO2+NaNO3+H2O
NO2+NO+2NaOH====2NaNO2+H2O
②氨催化还原法,反应原理是:
NOx+NH3![]() N2+H2O
N2+H2O
现有一定量的含NO2和NO的HNO3工业尾气(不含其他气体),若用过量的NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
(2)若1体积的该尾气用氨催化还原法处理,至少消耗多少体积相同状况下的氨气?
查看答案和解析>>
科目: 来源: 题型:022
如图所示装置是某种气体X的发生装置和收集装置(必要时可加热),所用的试剂从下列试剂中选取2~3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水。
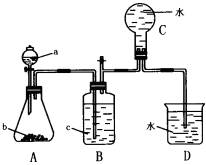
请回答下列问题:
(1)气体X的化学式是 。
(2)所选药品a是 ,b是 ,装置B的作用是 。
(3)用所选的药品发生反应生成X时,离子方程式是 。
(4)在反应刚开始时A中的主要现象是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com