
科目: 来源: 题型:022
在某些条件下,容器中有如下平衡反应:A + 4B![]() 2C + D + Q此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
2C + D + Q此时,A、B、C的物质的量均为a mol,而D的物质的量为d mol。
(1)改变a的取值,再通过改变反应条件,可以使反应重新达到平衡。并限定达到新的平衡时,D的物质的量只允许在![]() 到2d之间变化,则a的取值范围应是____________(用a和d的关系式表示)。
到2d之间变化,则a的取值范围应是____________(用a和d的关系式表示)。
(2)如果要使本反应重新建立的平衡中,D的物质的量只允许在d到2d之间取值,则应该采取的措施是( )
A.升高反应温度
B.增大反应容器内压强
C.增大反应容器容积
D.降低反应温度
E.减小反应容器内压强
F.减小反应容器容积
查看答案和解析>>
科目: 来源: 题型:022
Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu和Cu2+。现有浓H2SO4、浓HNO3、稀H2SO4、稀HNO3、FeCl3稀溶液及pH试纸,而没有其它试剂。简述如何用最简便的方法来检验CuO经氢气还原所得到的红色产物中是否含有碱性氧化物Cu2O。
查看答案和解析>>
科目: 来源: 题型:022
2003年用于“非典型性肺炎”消毒的高效、无污染消毒剂ClO2已经被许多发达国家广泛应用在饮用水的处理上。
(1)实验室制备ClO2的方法是用亚氯酸钠与氯气反应:2NaClO2+Cl2====2ClO2+2NaCl
反应中的氧化产物是______________。
(2)工业上制备ClO2的一种方法是用甲醇在酸性介质中还原氯酸钠。请配平下列反应方程式,并标出电子转移的方向和数目。
□CH3OH+□ NaClO3+ □H2SO4—— □ClO2+□CO2+□Na2SO4+□H2O
(3)若上述两个反应中转移了等量的电子,则两种方法制得的ClO2的物质的量这比为n(1):n(2)=______________。
查看答案和解析>>
科目: 来源: 题型:022
硝酸工业尾气中的氮的氧化物(NO、NO2)是主要的大气污染物之一,其常用的治理方法有以下几种:
①NaOH溶液吸收法,反应原理如下:
2NO2+2NaOH====NaNO2+NaNO3+H2O
NO2+NO+2NaOH====2NaNO2+H2O
②氨催化还原法,反应原理是:
![]()
![]()
![]()
现有一定量的含NO2和NO的HNO3工业尾气(不含其他气体),若用过量的NaOH溶液吸收后,溶液中NaNO3与NaNO2的物质的量之比恰好与尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
(2)若1体积的该尾气用氨催化还原法处理,至少消耗多少体积相同状况下的氨气?
查看答案和解析>>
科目: 来源: 题型:022
阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2 + O2 == 2H2O。试回答下列问题:
(1)若电解质溶液为KOH溶液,构成燃料电池,则电极反应式为: 。
(2)如把KOH改为稀H2SO4作导电物质,则电极反应式为: 。
(3)如把H2改为甲烷,KOH作导电物质,则电极反应式为: 。
查看答案和解析>>
科目: 来源: 题型:022
2000年,国家药品监督管理局发布通告暂停使用和销售含苯丙醇胺的药品制剂。苯丙醇胺(英文缩写为PPA)结构简式如下:

其中![]() 代表苯基。苯丙醇胺是一种一取代苯,取代基是
代表苯基。苯丙醇胺是一种一取代苯,取代基是 。
。
(1)PPA的分子式是: 。
(2)它的取代基中有两个官能团,名称是 基和 基(请填写汉字)。
(3)![]() 、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,其中5种的结构简式是:
、H2N-、HO-在碳链上的位置作变换,可以写出多种同分异构体,其中5种的结构简式是:
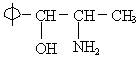 、
、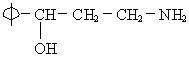 、
、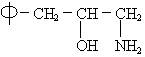 、
、
 、
、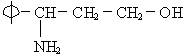
请写出另外4种同分异构体的结构简式(不要写出-OH和-NH2连在同一个碳原子上的异构体;写出多于4种的要扣分):
、 、 、 。
查看答案和解析>>
科目: 来源: 题型:022
(1)分离沸点不同但又互溶的液体混合物,常用什么方法?
(2)在分液漏斗中用一种有机溶剂提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。
查看答案和解析>>
科目: 来源: 题型:022
对于同一种物质,被氧化的程度越大,氧化剂的 性就越 ,例如Fe+S== FeS,2Fe+3Cl2==2FeCl3,则氧化性Cl2 S;对于同一种物质,被还原得越彻底,还原剂的 性就越 。例如:HCl+H2SO4(浓)→不反应、2HBr+ H2SO4(浓)= Br2+SO2↑+2H2O、8HI+H2SO4(浓)== 4I2+H2S↑+4H2O,则还原性HI HBr HCl。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com