
科目: 来源: 题型:022
Na2CO3溶液中滴加酚酞呈红色,原因是 (用离子方程式表示)。加热后颜色变 ,原因是 。若在该溶液中滴加过量的BaCl2溶液,所观察到的现象是 ,其原因是 (用离子方程式和简要的文字说明)。
查看答案和解析>>
科目: 来源: 题型:022
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据工艺流程图,完成下列填空。
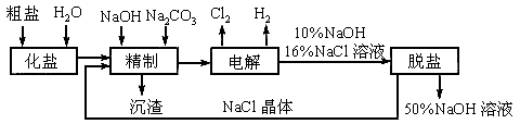
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
查看答案和解析>>
科目: 来源: 题型:022
某学生中和滴定实验的过程如下:
(a)取一支碱式滴定管
(b)用蒸馏水洗净,
(c)加入待测的NaOH溶液,
(d)记录液面刻度的读数
(e)用酸式滴定管精确放出一定量标准酸液,
(f)置于未经标准液润洗的洁净锥形瓶中,
(g)加入适量蒸馏水,
(h)加入2滴酚酞试液,
(i)开始滴定,边滴边摇荡,
(j)边注视滴定管内液面变化,
(k)当小心滴到溶液由无色变成粉红色时,即停止滴定,
(l)记录液面刻度的读数,
(m)根据滴定管的两次读数得出NaOH溶液的体积为22 mL。
指出上述实验过程中的错误之处(用编号表示):
。
查看答案和解析>>
科目: 来源: 题型:022
有FeCl2、CuCl2混合溶液400 ml,经测定,其中[Cl-]为a mol/L,投入b g锌粉(过量),充分反应后,过滤,所得固体残渣经洗涤、干燥后,质量为c g。(只考虑金属与盐的反应)。
(1)原混合溶液中Fe2+、Cu2+的物质的量浓度为[Fe2+]=________;[Cu2+]=________。
(2)b>________a。
(3)c的数值越大,说明混合溶液中CuCl2含量________。
(4)c的取值范围为________(以a、b表示)。
查看答案和解析>>
科目: 来源: 题型:022
用酸碱中和滴定法测定某氢氧化钠溶液的浓度时,取等体积的两份待测碱液,其中一份已在空气中敞口放置一段时间,此溶液的pH要 (增大、减小、不变)原因是 。若用标准硫酸溶液滴定上述曾在空气中放置一段时间的一份氢氧化钠溶液,消耗标准酸液体积为V1,滴定未敞口放置的另一份氢氧化钠溶液,消耗标准酸液体积为V2,那么:⑴以甲基橙为指示剂时,V1和V2的关系是 ;⑵以酚酞为指示剂时,V1和V2的关系是 。
查看答案和解析>>
科目: 来源: 题型:022
⑴称取m g纯净的NaCO3固体,跟20 mL盐酸恰好完全反应生成NaCl,CO2和H2O则该盐酸的物质的量浓度为
⑵如上述m g Na2CO3样品中,实际上混有一种杂质(可能是NaCl,NaOH或K2CO3),当盐酸的实际浓度大于⑴中计算所得数值时,则Na2CO3所含杂质是 。结合必要的数据简述理由。
查看答案和解析>>
科目: 来源: 题型:022
用已知浓度的强酸滴定未知浓度的强碱时。下列操作对测定结果的影响,用“偏低、偏高、不影响”填空。
⑴酸式滴定管,用蒸馏水洗后,未用标准液润洗 ;
⑵碱式滴定管,用蒸馏水洗后,未用待测液润洗 ;
⑶滴定前酸式滴定管尖嘴处未充满溶液 ;
⑷取待测碱液时,碱式滴定管尖嘴处未充满溶液 ;
⑸锥形瓶用蒸馏水洗净后,未把水倒净,就直接用来盛放待测碱液 ;
⑹锥形瓶有蒸馏水洗净后,又用待测液润洗 ;
⑺滴定过程中振荡锥形瓶时溅出了一些待测的碱液 ;
⑻滴定则达终点时立即读数 ;
⑼滴定完毕后,滴定管下端尖嘴处留有液滴 ;
⑽读取标准溶液体积时,滴定前仰视,滴定后俯视 ;
⑾用酚酞作指示剂,当红色褪成无色,又滴一滴NaOH,无颜色变化 。
查看答案和解析>>
科目: 来源: 题型:022
将0.02 mol•L-1的HCN与0.02 mol•L-1NaCN溶液等体积混合,已知该混合溶液中![]() ,用“>、<或=”填空。
,用“>、<或=”填空。
⑴![]() 。
。
⑵c(HCN) c(CN--)
⑶c(HCN)+c(CN-)_______0.02 mol•L-1。
查看答案和解析>>
科目: 来源: 题型:022
25℃时,若体积为Va、pH=a的某一元强酸与体积为Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a>0.5b,请填写下列空白:
⑴a值可否等于3(填“可”或“否”) ,其理由是_______________。
⑵a值可否等于5(填“可”或“否”) ,其理由是_______________。
⑶a的取值范围是 。
查看答案和解析>>
科目: 来源: 题型:022
某地的酸雨中,含c(Na+)=7.0×10-6mol•L-1,c(Cl-)=4.5×10-5mol•L-1,c(NH4+)=2.3×10-5mol•L-1,c(SO![]() )=2.5×10-6mol•L-1,则该地酸雨的pH约为 。
)=2.5×10-6mol•L-1,则该地酸雨的pH约为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com