
科目: 来源: 题型:022
现有如下各实验:
A.将1g KCl加入10g沸腾的水中
B.将1g可溶性淀粉加入到100g水中,搅拌均匀后煮沸
C.将1g白磷加入到100g CS2中,充分振荡
D.将1g CaCO3粉末加入100g水,充分振荡
E.将0.1g植物油加入到10g水中,充分振荡混匀
F.将96mL乙酸与5mL水充分混合
上述实验中所得到的分散系,属于溶液的有________;属于胶体的是________;属于浊液的是________。
查看答案和解析>>
科目: 来源: 题型:022
两元素A、B能形成AB2型化合物,AB2共有38个电子,若AB2为离子化合物时,其化学式是________________,电子式是________________;若AB2为共价化合物时,其分子式是________________,结构式为________。
查看答案和解析>>
科目: 来源: 题型:022
向①少量MgCl2溶液;②少量AlCl3溶液中都分别先加入少量、再加入过量的NaOH溶液,振荡
(1)观察到的现象分别是① ,② 。
(2)有关离子方程式是① ②
(3)由上述现象可得到的结论是 ,碱性顺序Mg(OH)2 Al(OH)3,金属性顺序Mg Al。
查看答案和解析>>
科目: 来源: 题型:022
从①渗析、②盐析、③溶胶、④布朗运动、⑤电泳、⑥丁达尔效应、⑦中和、⑧水解中,选出适当的词语填入下列每小题的空格中(填编号)。
(1)在肥皂水中透过强光,可以见到“光带”。这种现象称为________;
(2)在浓的肥皂水中加入饱和食盐水(或固体食盐)肥皂凝聚。这种现象称为________;
(3)在显微镜下观察到花粉的运动称为________;
(4)在肥皂水中加入酚酞变成红色,说明高级脂肪酸根离子发生了________;
(5)用半透膜把Fe(OH)3胶体中含有的NaCl分离出去的方法叫做________。
查看答案和解析>>
科目: 来源: 题型:022
由主要成分是碳酸钡、碳酸钙组成的矿石样品,某课外活动小组欲从该样品中分离出碳酸钡,并尽可能除去Ca2+。供实验参考的数据见下表。
|
溶解度
物质 |
0℃ |
50℃ |
80℃ |
|
Ca(OH)2 |
0.173g |
0.130g |
0.094g |
|
Ba(OH)2 |
1.64g |
13.1g |
101.5g |
分离过程中用到的试剂有:矿石,水,不能再用其他试剂;要求将矿石经如下四步反应或操作后得到较纯净的碳酸钡。
![]()
试回答下列问题:
(1)在括号中填入实验的条件或方法:①________,②________。
(2)在方框中填入相应物质的化学式:b________,c________。
(3)写出有关反应的化学方程式:
b→c:________。
c→BaCO3:________。
查看答案和解析>>
科目: 来源: 题型:022
化合物A、D、F是中学化学中常见的物质,化合物B、C、E中含有两种相同的元素。这些化合物之间存在如图的关系。其中A和B的反应是一种重要化工生产中的主要反应之一。
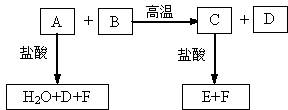
(1)在A、C、F中含有相同的元素是________;
(2)化合物C的化学式是________,化合物A的水溶液显________性(填“酸”、“碱”或“中”)。
(3)C的水溶液和D能否发生反应?________,其理由是 。
查看答案和解析>>
科目: 来源: 题型:022
镁是很活泼的金属,常用做脱硫剂,脱氧剂。在电子工艺中利用镁制取硅的反应为:2Mg+ SiO2![]() 2MgO+Si,△H=-372kJ•mol-1,同时有副反应:2Mg+Si
2MgO+Si,△H=-372kJ•mol-1,同时有副反应:2Mg+Si![]() Mg2Si发生。Mg2Si遇盐酸迅速反应生成硅烷(SiH4),SiH4常温下是一种不稳定,易分解的气体。
Mg2Si发生。Mg2Si遇盐酸迅速反应生成硅烷(SiH4),SiH4常温下是一种不稳定,易分解的气体。

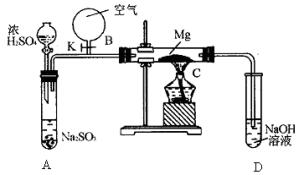
甲 乙
(1)如图甲所示是进行Mg与SiO2反应的实验装置。
①由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气。X气体应为________(镇标号)。
A.H2 B.N2 C.CO2
②实验开始时必须先通入X气体后,再接通电源加热反应物,其理由是________,当反应引发后,切断电源,反应能继续进行,其理由是________
③反应结束后,待冷却至常温后,关闭K,从分液漏斗处加稀盐酸,可观察到导管口A处有闪亮的火星,据此可推知SiH4的性质________。
(2)用图乙所示装置的实验如下:先关闭K,使A中反应进行,加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质。实验完成后将C管中固体全部加入盐酸中,有腐蛋味气体生成。
①C中Mg应放在不锈钢垫片上,而不能直接接触试管壁,这是因为________。
②停止实验时,先打开K,再停止滴加浓H2SO4,最后熄灭酒精灯。橡胶气胆B在实验中的作用是________。
③C中全部产物有________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:022
熔融盐燃料电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气体为阴极助燃气,制得在650℃下工作的燃料电池。完成上述有关的电池反应式。
阳极反应式:2CO+2CO![]() ==4
==4![]() ↑+4e-;
↑+4e-;
阴极反应式: ;
总电池反应式: ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com