
科目: 来源: 题型:022
某元素R具有微弱放射性,其原子核内中子数比质子数多43。由R组成的固体单质A,在一定条件下密度为6.88g•cm-3。用X射线研究固体A表明,在边长为1.00×10-7cm的立方体中含有20个原子。R在化学反应中常表现为+2价、+4价。在溶液中R2+稳定,而R4+有强氧化性,可将NO氧化为HNO3。氧化物R3O4其性质与Fe3O4有些类似。R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈。R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途。请回答:
(1)R原子的摩尔质量为________。
(2)R元素处于周期表中________周期________族。
(3)假若使少量R4+加到Fe(NO3)2溶液中,是否会发生反应?若“否”,说明原因;若“是”,请写出离子方程式________。
(4)R3O4因具有氧化性,被大量用于油漆涂料,涂在钢铁表面,有利于形成耐腐蚀的钝化层。R3O4与足量HNO3反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________。
查看答案和解析>>
科目: 来源: 题型:022
有甲、乙、丙、丁四种液体,它们分别为Fe(OH)3胶体、硅酸溶液、As2S3胶体、NaOH溶液。现将有关试验现象记录如下:①电泳:甲液体的阳极周围颜色变浅,阴极周围颜色变深;②将一束光通过乙液体,无丁达尔现象;③将乙慢慢加入到丙液中,先出现聚沉,后液体变清,则甲为________,乙为________,丙为________,丁为________。
查看答案和解析>>
科目: 来源: 题型:022
银器皿日久表面逐渐变黑色,这是由于生成硫化银,有人设计用原电池原理可除去硫化银,其处理方法为:将一定浓度的食盐溶液注入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银不会损失。试回答:在此原电池反应中,负极发生的反应为 ,正极发生的反应为 ,反应过程中产生臭鸡蛋气味,原电池总反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:022
乙烯基乙炔(CH2=CH―C≡CH)是一种重要的不饱和烃,其分子里最多有________个原子在同一条直线上;最多有________个原子在同一平面内.
查看答案和解析>>
科目: 来源: 题型:022
A是一种酯,化学式是C14H12O2,A可以由醇B跟羧酸C发生酯化反应得到。A不能使溴(CCl4溶液)褪色,氧化B可得到C。
(1)写出A、B、C的结构简式:A_________,B_________,C_________。
(2)写出B的两种同分异构体的结构简式(它们都可以跟NaOH反应):_________和_________。
查看答案和解析>>
科目: 来源: 题型:022
F2、Cl2、Br2、I2的熔点依次增高,而分子的热稳定性却依次减弱,原因是_____________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:022
在淀粉—KI溶液中,滴入少量NaClO溶液,并加入少量硫酸,溶液立即变蓝,这是因为
,离子方程式是
。在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失,这是因为
,离子方程式是
。从以上实验可知,ClO-、![]() 、SO
、SO![]() 的氧化性由强到弱的顺序是 。
的氧化性由强到弱的顺序是 。
查看答案和解析>>
科目: 来源: 题型:022
在半导体工业中,有一道工序叫烧氢。烧氢的工艺流程如图所示。工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。
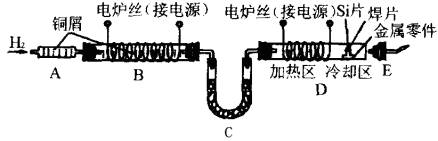
试回答下列问题:
(1)装置B的作用是________;B中发生反应的化学方程式是________。
(2)装置C中的物质是________;C的作用是 。
(3)点燃氢气前将E(带导管胶塞)接在D出口处,目的是________。
(4)装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com