
科目: 来源: 题型:022
苯环上原有取代基对苯环上再导入另外取代基的位置有一定影响。其规律是(1)
苯环上新导入的取代基的位置主要决定于原有取代基的性质;(2)可以把原有取代基分为两类:①原取代基使新导入的取代基进入苯环的邻、对位,如—OH,—CH3(或烃基),—C1,—Br,—O—COR等,②原取代基使新导入的取代基进入苯环的间位,如—NO2,—SO3H,—CHO等。现有下列变化(反应过程中每步只能引进一个新的取代基):
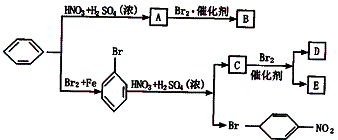
请写出其中一些物质的主要结构简式:
( )
A. _______
B. _______
C. _______
D. _______
查看答案和解析>>
科目: 来源: 题型:022
已知烯烃、炔烃,经臭氧作用发生反应:
CH3—CH![]() CH—CH
CH—CH![]() CH2
CH2![]() CH3CHO+OHC—CHO+HCHO,
CH3CHO+OHC—CHO+HCHO,
CH3—C![]() C—CH2—C
C—CH2—C![]() CH
CH![]() CH3COOH+HOOC—CH2—COOH+HCOOH,
CH3COOH+HOOC—CH2—COOH+HCOOH,
某烃分子式为C10H10,在臭氧作用下发生反应:
C10H10![]() CH3COOH+3HOOC—CHO+CH3CHO,试回答:
CH3COOH+3HOOC—CHO+CH3CHO,试回答:
①C10H10分子中含________个双键,________个三键;②C10H10的结构简式为________。
查看答案和解析>>
科目: 来源: 题型:022
已知(1)Cu2+、Fe2+在PH为4~5的条件下不水解,而这一条件下Fe3+几乎 全部水解。(2)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O。
现用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液的过程如下:①取50mL纯净的盐 酸,加入一定量的粗CuO加热搅拌、充分反应后过滤,测知滤液的PH=3 ②向滤液中加入双氧水、搅拌 ③调节②中溶液的PH至4,过滤 ④把③所得滤液浓缩 回答以下问题:
(1)②中发生反应的离子方程式是________。
(2)③中使PH升高到4,采取的措施是加入过量的________,并微热、搅拌
A.NaOH
B.氨水
C.CuCl2
D.CuO(3)
③中过滤后滤渣的成分是________。
查看答案和解析>>
科目: 来源: 题型:022
一包白色固体,可能由NaOH、NaCl、Na2CO3、Na2SO4、NaNO3、CuSO4中的一种或几种组成,为判断其组成,作了如下实验:
②取少量固体,加入浓硫酸和铜屑,微热后有红棕色气体产生; ③取少量固体,加入浓硫酸,微热时有气体产生,该气体不能使澄清石灰水变浑浊; ④取少量固体,溶于水后,加过量硝酸钡溶液,有白色沉淀生成,再继续滴加硝酸银 溶液,沉淀又增加。
(1)该样品中一定含有的物质是________,一定不含的物质是________;可能含有的 物质是________。
(2)写出②和③实验中有关反应的化学方程式:________________ ②中________,③中________________
查看答案和解析>>
科目: 来源: 题型:022
现有A、B、C、D四种气体,都是无机物,能发生下列反应:
A+D→E+H![]() O E+O
O E+O![]()
![]() D C+D→B+F B+O
D C+D→B+F B+O![]() →C 其中:C为红棕色,D能使石灰水变浑浊,E常温下是固体,F是一种酸酐。
→C 其中:C为红棕色,D能使石灰水变浑浊,E常温下是固体,F是一种酸酐。
(1)写出这四种气体的化学式:A________,B________,C________,D________。
(2)写出C+D—B+F的反应方程式________________。
查看答案和解析>>
科目: 来源: 题型:022
盖斯定律可以简单地归纳为“如果一个反应可以分几步进行,则各分步反应反应热之和与该反应一步完成时的反应热是相同的”。
应用盖斯定律完成下面的计算:
在101kPa、25℃时,lmol某烷完全燃烧生成CO2和H2O,放出5518kJ的热量。并测 得以下三个反应热:
①nC(s)+(n+1)H2(g)=CnH2+2;△H:-202kJ·mol-1 ②nC(s)+O2(g)=CO2;△H=-393.5kJ·mol-1 ③H2(g)十1/2O2(g)=H2O(1);△H=-285.8kJ·mol-1(1)试求n值。
(2)写出该烷烃燃烧的热化学方程式___________________。
查看答案和解析>>
科目: 来源: 题型:022
请按要求填空。
(1)用已准确称量的1.06gNa2CO3固体配制0.100mol·L-1 Na2CO3溶液100mL,所需仪器为________。
(2)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。
(3)除去KCl溶液中的![]() ,依次加入的溶液为(填溶质的化学式)________。
,依次加入的溶液为(填溶质的化学式)________。
查看答案和解析>>
科目: 来源: 题型:022
(重组提高)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时即产生大量氮气和水蒸气,并放出大量的热。已知:0.4mol液态肼与足量的双氧水反应,生成氮气和水蒸气,并放出256.65KJ的热量。
(1)反应的热化学方程式________。
(2)又已知:H2O(1)=H2O(g);△H=-44kJ·mol-1,则16g液态肼与液态双氧水反应生成液态水时放出的热量是________。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是________。
查看答案和解析>>
科目: 来源: 题型:022
(2004年春季高考题)X、Y、Z三种元素位于周期表前20号元素之中:已知:①XY2加水生成Y2Z2和化合物D;②X的氧化物加水也生成D;③Y的氧化物 有两种。
请填空:(1)X、Y、Z的元素符号为X________,Y________,Z________。
(2)反应①的化学方程式为(3)反应②的化学方程式为
查看答案和解析>>
科目: 来源: 题型:022
A、B、C、D、E分别是铁的单质或铁的化合物,其相互反应关系如下图所示:
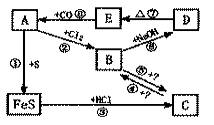
根据上图所示变化,要求回答:
(1)推断A、B、C、D、E各是什么物质。
A________、B________、C________、D________、E________;(2)写出各步反应的化学方程式:
①________;②________; ③________:④________; ⑤________;⑥________; ⑦________;⑧________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com