
科目: 来源:物理教研室 题型:022
![]()
(1)请完成该化学方程式并配平(未知物化学式和系数填入框内)
(2)浓盐酸在反应中显示出来的性质是______ (填写编号、多选倒扣)
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(3)产生
![]() 则转移电子的物质的量为
mol
则转移电子的物质的量为
mol
(4)
![]() 具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是
具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是
![]() 倍。
倍。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
c(Na+)=0.0014 mol·L-1 c(Cl-)=0.0035 mol·L-1
c(NH4+)=0.0023 mol·L-1 c(SO42-)=0.00015 mol·L-1
求该溶液中的氢离子的物质的量浓度?
查看答案和解析>>
科目: 来源:物理教研室 题型:022
|
测试时间(小时) |
0 |
1 |
2 |
4 |
8 |
|
雨水的pH |
4.73 |
4.62 |
4.56 |
4.55 |
4.55 |
雨水的pH变小的原因是 。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
②B不完全燃烧时生成淡黄色粉末C;
③C在空中燃烧呈现淡蓝色火焰,并生成有刺激性气味的气体D;
④将D通入到Ba(OH)2溶液中生成白色沉淀E;
⑤过滤后将E溶于HCl中,又生成气体D;
⑥D与B反应又生成淡黄色粉末C;
⑦将C与铁粉共热,又生成固体A。
从以上事实可知各物质的分子式为:
A ,B_______________,C________________,D ,E_______________。
各步反应的化学方程式为:
① ;
② ;
③ ;
④ ;
⑤ ;
⑥ ;
⑦ 。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
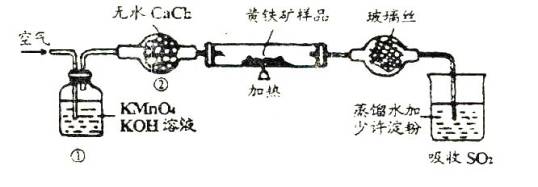
A. 将试管中的样品加热到800—850℃
B. 称取研细的黄铁矿样品
C. 连接全部仪器,使其成为整套试验装置,并检查气密性
D. 将样品小心放入容器中,在将容器小心地推入试管中部
E. 以每分钟1 L的速度鼓入空气
F. 用标准碘液滴定含淀粉的SO2水溶液
(1)正确的试验步骤,其操作编号是 。
(2)装置(1)的作用是 ;装置(2)的作用是 。
(3)碘液跟二氧化硫水溶液发生反应的化学方程式是 。
(4)假定矿样品的硫全部转化为二氧化硫,并全部被水吸收。若称得矿样的质量是0.12克,滴定管中最初读数为0.10mL,末读数为25.60mL,标准碘液的浓度为0.05摩/升,则黄铁矿样品种的含硫量是(列式及答案) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com