
科目: 来源:物理教研室 题型:022
|
|
A |
|
|
|
B |
|
|
C |
(1)元素名称:A________,B________,C________。
(2)A原子的结构示意图:________,C的阴离子结构示意图:________。
(3)B单质的晶体类型为________,C单质的晶体类型为________。
(4)A的氢化物的化学式为________,结构式为________,在该氢化物中,A的原子与H原子是以________键结合的。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
已知:①A++C-=D+E↑; ②B++C-![]() 2D。
2D。
(1)C-离子的电子式是________。
(2)具有相同空间构型的粒子是________和________,A+离子中的键角为________。
(3)分别写出A+和D反应、B+和E反应的离子方程式。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)A、B、E、F四种元素组成的一种化合物的名称是:
(2)D、F两种元素最高价氧化物对应的水化物之间发生反应的化学方程式是___ ___ __ 。
(3)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为_____ ___ 。
(4)若以上(2)、(3)两个反应中反应物间恰好完全反应,且得到等体积、等物质的量浓度的溶液,则(2)、(3)反应所得溶液中的离子个数是(2)________(3)(空格内选填“大于”、“小于”或“等于”)
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
|
物质 |
NaF |
NaCl |
NaBr |
NaI |
NaCl |
KCl |
RbCl |
CsCl |
|
熔点/℃ |
995 |
801 |
755 |
651 |
801 |
776 |
715 |
646 |
|
物质 |
SiF4 |
SiCl4 |
SiBr4 |
SiI4 |
SiCl4 |
GeCl4 |
SnCl4 |
PbCl4 |
|
熔点/℃ |
-90.2 |
-70.4 |
5.2 |
120.5 |
-70.4 |
-49.5 |
-36.2 |
-15.0 |
(1)钠的卤化物及碱金属的氯化物的熔点与________有关,随________增大________减小,故熔点依次降低。
(2)硅的卤化物及硅、锗、锡、铜的氯化物的熔点与________有关,随着________增大________增大,故熔点依次升高。
(3)钠的卤化物的熔点比相应的硅的卤化物的熔点高得多,这与________有关,因为________故前者熔点远远高于后者。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)只有非极性键的是________。
(2)只有极性键的是________。
(3)既有极性键又有非极性键的是________。
(4)只有离子键的是________。
(5)既有离子键又有极性键的是________。
(6)既有离子键又有非极性键的是________。
(7)无任何化学键的是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
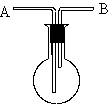
(1)当烧瓶干燥时从A口进气可收集的气体是____ ____;以B口进气可收集的气体是_____ ___。
(2)当烧瓶充满水时,可用来测量_______ _等气体的体积,气体从________口进入。
(3)当烧瓶中装入洗液用于洗气时,气体应从________口进。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)画出这两种固体分子的几何构型图(指明各是哪一种)。
(2)已知PtCl2(NH2)2能被Cl2氧化成PtCl4(NH2)2,其空间结构是以Pt原子为中心的八面体,其中在水中溶解度较小的PtCl4(NH2)2的结构为________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.98 |
1.57 |
2.04 |
2.25 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)推测在同周期或同主族的元素中x值与原子半径的关系是________。根据短周期元素的x值变化特点,体现了元素性质的________变化规律。
(2)通过分析x值变化规律,确定Mg、N的x值范围:________<x(Mg)<________,________<x(N)<________。
(3)在P-N键中,共用电子对偏向________原子;
(4)经验规律告诉我们:当成键的两原子相应元素的x差值(Dx)即Dx>1.7时,一般为离子键,Dx<1.7,一般为共价键,试推断:AlBr3中化学键类型是________。
(5)推测元素周期表中,x值最大的元素是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)写出它的电子式和结构式____ ___。
(2)指出分子内的化学键类型____ ____。
(3)指出二氯化二硫中硫元素的化合价________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com