
科目: 来源:物理教研室 题型:022
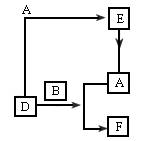
(1)D、E、F化合物中含有甲元素的是_____________________。
(2)上述反应中,单质B是___________(填氧化剂,还原剂或催化剂)。
(3)如果甲是非金属元素,则E的化学式是_____________,D的电子式是
_____________________________。
(4)如果甲是金属元素,写出D与B反应的化学方程式__________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)在温度T℃和压力为pPa的情况下,1.95gA与11.0g 恰好完全反应,生成固体C和3.00L的D气体,计算生成C的质量(m)。
缺少的数据是:__________;
计算式为m=___________。
(2)0.48g金属Mg与10mL HCl反应,计算生成的H2在标准状况下体积V(H2)。
缺少的数据是:______________________;
计算式为:_________________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入少量CO4及数滴氯水,振荡后CCl4层为紫红色;
(3)另取部分溶液,逐渐加入稀NaOH溶液,使溶液从酸性转为碱性,在滴加过程中及滴加完毕,均无沉淀生成;
(4)取上述碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
(5)取(3)得到的碱性溶液加热,加Na2CO3溶液,有白色沉淀生成。
根据实验事实确定上述离子中:
在溶液中肯定存在的有__________________;
在溶液中肯定不存在的有_________________;
在溶液中不能确定是否存在的有________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(2)水俣病的祸根是__________有害物质。
(3)服用FeSO4制剂的病人,不宜__________,因为___________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)称取10.00g样品,将其加入过量的NaOH浓溶液中共热并蒸干,AlN跟NaOH溶液反应生成NaAlO2,并放出氨气3.36L(标准状况)。
①上述反应的化学方程式为____________。
②该样品中的AlN的质量分数为__________。
(2)另取10.00g样品置于反应器,通入2.016L(标准状况)O2,在高温下充分反应后测得气体的密度为1.34g×L-1(已折算成标准状况,AlN不跟O2反应)。该样品中含杂质炭_________g。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
实验序号 甲 乙 丙
合金质量/g 0.255 0.385 0.459
生成气体/mL 280 336 336
试回答:
(1)甲组实验中盐酸_________,乙组实验中盐酸_________(填“过量”或“适量”或“不足量”)。
(2)要推导出盐酸的物质的量浓度,所提供的数据中作计算依据的是_________,计算出盐酸的物质的量浓度为_________mol×L-1。
(3)要求出合金中镁、铝的物质的量之比,可作计算依据的数据是_________,镁、铝的物质的量之比为__________。
(4)在丙组实验之后,向容器中加入一定体积1mol×L-1的苛性钠溶液,可恰好使铝元素全部以偏铝酸根形式存在,并使镁离子刚好完全沉淀,则溶液中偏铝酸钠的物质的量为__________mol,氯化钠的物质的量为_________mol,所加苛性钠溶液的体积为__________mL。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)求所需三种肥料的质量。
(2)当植物在其中生长一段时间后,溶液的pH有何变化?说明原因。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com