
科目: 来源:物理教研室 题型:022
(1)A的分子式是________,其结构简式是
________________________________________________。
(2)写出A与乙酸反应的化学方程式:
________________________________________________________。
(3)写出满足下列3个条件的A的同分异构体的结构简式。①属直链化合物;②与A具有相同的官能团;③每个碳原子上最多只连一个官能团。这些同分异构体的结构简式是________________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022

②R—CH2—X+H2O![]() R—CH2OH+HX
R—CH2OH+HX
现有含C、H、O的有机化合物A~F,相互之间的转化关系如图:

(1)化合物A~F相互转化的关系中,属于取代反应的有________(写出反应序号)
(2)化合物A和F的结构简式分别为:A______________________________________;
F__________________________________________________________________________。
(3)写出E与足量D在浓H2SO4作用下反应的化学方程式。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
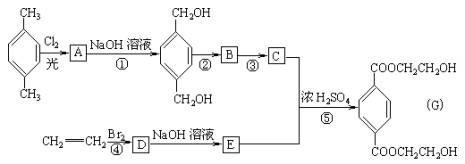
(1)写出结构简式A________,B________,C________,E________。
(2)反应类型①________,②________,③________,④________,⑤________。
(3)写化学方程式:C+E![]() G___________________________________________,
G___________________________________________,
C和E生成高分子化合物________________________________________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
________________________________________________________
________________________________________________________
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)淡黄色粉末名称是________。
(2)溶液中肯定有________离子;肯定没有________离子。
(3)溶液中离子的物质的量之比是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
熔块,过滤弃去残渣,滤液用盐酸酸化,经分离分别得到沉淀和溶液,溶液即为净水剂。
(1)写出熔融时主要成分与纯碱反应的化学方程式(Al2O3与纯碱反应跟SiO2与纯碱反应相似)_________________________。
(2)最后的沉淀是__________,生成沉淀的离子方程式是______________________。
(3)实验室中常用的有瓷坩埚、氧化铝坩埚和铁坩埚,本实验在熔融土样时,应选用_________坩埚。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)H2SO4溶液的物质的量浓度为________。
(2)若b=2.75mL,则铝土矿中各成分的质量分数是________。
(3)b值的范围在________之间,在这个范围内,b值越大,________的含量越少。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com