
科目: 来源:物理教研室 题型:022

请回答下列问题:
(1)配平反应①的离子方程式(配平系数填入相应的方框内).
(2)用Na2S2O3标准液滴定I2时(反应④)选用的指示剂是________.
(3)取b0mL待测液,用H2SO4酸化,再用a1mol·L-1的标准KMnO4溶液滴定其中的H2O2,耗用KMnO4体积b1mL,(滴定过程中KMnO4不与![]() 反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
反应)另取b0mL待测液,加入过量KI,用H2SO4酸化,
此时![]()
与H2O2都能与KI反应生成I2(反应②和③).再用a2mol·L-1Na2S2O3标准液滴定生成I2,耗用Na2S2O3为b2mL.
请根据上述实验数据计算过氧乙酸浓度(用含a1,a2,b0,b1,b2的代数式表示).c0=___________
(4)为计算待测液中![]() 浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
浓度c0,加入KI质量已过量但没有准确称量,是否影响测定结果________(填是或否).
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)写出A→E的分子式
A________ B________ C________ D________ E________
(2)写出指定反应的化学方程式

①B→C________________________
②E→C________________________
③C→D________________________
查看答案和解析>>
科目: 来源:物理教研室 题型:022
①固体A属于________晶体,它的电子式为________.
②A溶于水后溶液呈________性(填“酸”“碱”或“中”),其原因用化学方程式表示为____________________.
③A受热分解的化学方程式__________________.
(2)A与铜或铜的某些化合物在一定条件下可合成CuH.CuH是一种难溶物,它能在Cl2中着火,还能与HCl反应放出气体,写出这两个反应的化学方程式①__________________②____________________.
(3)工业上制CuSO4时,不用Cu与浓H2SO4直接反应而是将铜丝浸在稀H2SO4中,再不断由容器下部吸入细小的空气泡,这样做的好处是①________________②___________.
相同元素不同化合价间转化.
查看答案和解析>>
科目: 来源:物理教研室 题型:022

依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是________________________.
(2)nmol CH4经一次转化后产生CO 0.9 nmol,产生H2________mol(用含n的代数式表示).
(3)K2CO3溶液和CO2反应在加压下进行,加压的理论依据是________(多选扣分).
(a)相似相溶原理
(b)勒夏特列原理
(c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于________________(写出CO2的一种重要用途).
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3溶液循环,请在上述流程图中标出第三处循环(循环方向,循环物质).
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)下面是某化学课外小组的同学提出的实验室制备氨气的几种方案,其中可行的是( )
A.硫酸铵固体和消石灰共热 B.浓氨水逐滴加到新制的生石灰中
C.在一定条件下N2与H2化合 D.加热分解氯化铵固体
(2)该小组同学设计的制备氮化镁的方案有以下两个.分别见实验方案的装置图1和图2(夹持及加热仪器没有画出.且在实验前系统内的空气均已排除)
〔方案一〕

图1
①该实验完成后,能否得到纯净的氮化镁________(填“能”或“不能”);简述理由________________________.
②装置C的作用是________.
〔方案二〕

图2
已知:6NH3+3Mg=3Mg(NH2)2+3H2↑
③该方案中存在的主要问题是________________________.
④如何才能解决上述问题________________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
①Y+NaOH→G+Q+H2O
②Z+NaOH→Q+X+H2O
③Q+H2O![]() X+H2↑
X+H2↑
④G→Q+NaCl
由以上各反应可判断:
(1)这五种化合物中,氯元素价态由低到高的顺序为:_______________________.
(2)由反应③可以看出Q、X中氯元素价态高低顺序,其依据是__________________.
(3)臭氧(O3)与二氧化氯作用,可得到红色油状的六氧化二氯(Cl2O6),遇到有机物时会爆炸.它与碱溶液作用可得到等物质的量的氯的两种含氧酸盐,代表该反应的是(填①~④编号)________,其离子方程式是__________________.
(4)亚氯酸盐(如NaClO2)可用作漂白剂,在常温下不见光时可保存约1年.但在酸性溶液中因生成亚氯酸而发生分解:5HClO2====4ClO2+H++Cl-+2H2O.分解时,刚加入硫酸时反应缓慢,随后突然反应迅速,释放出气态的二氧化氯,这是因为________(填序号).
①酸性亚氯酸的氧化性增强
②溶液中H+起催化作用
③溶液中Cl-起催化作用
④逸出ClO2使反应的生成物浓度降低
查看答案和解析>>
科目: 来源:物理教研室 题型:022

(1)图甲表示溶液中________离子变化曲线.
(2)对溶液进行导电实验,当通入混合气体的体积大于V1时,引起溶液导电性明显增强的主要阴阳离子为________.
(3)当n=0.02mol时,光照前混和气体中H2与Cl2物质的量之比为________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
a.PCl3在热水中水解,产物有H3PO3,结构式为:
b.H3PO3与NaOH反应,只生成Na2HPO3和NaH2PO3两种盐
c.H3PO3能使碘水褪色,再加入过量AgNO3溶液,生成黄色沉淀M,过滤后再加入CaCO3粉末,又生成黄色沉淀N
d.向H3PO3溶液中加AgNO3溶液,有黑色Ag和棕色气体生成
(1)H2PO3是________元________酸(填“强”或“弱”),具有________性(氧化或还原),与以上判断对应信息分别是a~d中的________、________.
(2)信息c中M是(填化学式)________,N是________,确证M与N是否是同一物质的理论依据是________.
(3)H3PO3与AgNO3溶液反应的化学方程式为_________________,被还原元素为________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
②x在A、B、C、D中都不呈现它的最高化合价.
③室温下单质A与某种常见一元强碱溶液反应可得到B和C.
④化合物D受热催化分解,可得元素Y的单质.
回答下列问题:
(1)元素X是________,Z是________.
(2)写出③中反应的化学方程式________________________.
(3)写出④中反应的化学方程式________________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
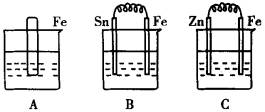
(1)A中反应的离子方程式为________________________.
(2)B中Sn极的电极反应式为________________________,Sn极附近溶液的pH(填“增大”“减小”或“不变”)________.
(3)C中被腐蚀的金属是________,总反应式为________.比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________.
非金属元素及其化合物有关计算.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com