
科目: 来源:物理教研室 题型:022
 合成时用了三种单体,这三种单体的结构简式为:
合成时用了三种单体,这三种单体的结构简式为:
ABS
CH2==CHCN、__________、__________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
 ClCH2COOH
ClCH2COOH
2,4,5-三氯苯酚 氯乙酸
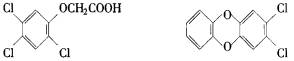
2,4,5-三氯苯氧乙酸 TCCD
请写出:
①生产2,4,5-三氯苯氧乙酸的化学方程式_______________________.
②由2,4,5-三氯苯酚生成TCDD反应的化学方程式:____________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
①
②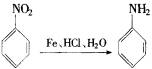 (苯胺 弱碱性、易氧化)
(苯胺 弱碱性、易氧化)
③![]()
利用这些反应,按以下步骤可以从某烃A合成一种染料中间体DSD酸.
![]()

(DSD酸)请写出A、B、C、D的结构简式.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
![]() ,当甲醛足量,另—醛中a
-H可继续发生上述反应直至a -H消耗完.又知无a
-H的醛可发生下列氧化反应:—CHO+—CHO
,当甲醛足量,另—醛中a
-H可继续发生上述反应直至a -H消耗完.又知无a
-H的醛可发生下列氧化反应:—CHO+—CHO![]()
—COO-+CH2OH,若把两种没有a -H的醛混合,发生氧化还原反应时,还原性强的醛使对方还原成醇,而自身被氧化成羧酸.甲醛在醛中还原性最强.
请用中学教材中学过的醛制备季戊四醇 (油漆和工程塑料的原料),写出其制备过程中发生反应的化学方程式(有机物用结构简式表示).
(油漆和工程塑料的原料),写出其制备过程中发生反应的化学方程式(有机物用结构简式表示).
查看答案和解析>>
科目: 来源:物理教研室 题型:022
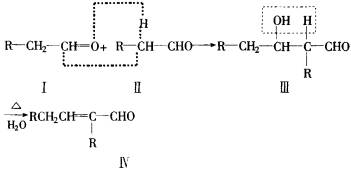
请运用学过的知识和上述信息写出由乙烯制正丁醇各步反应的化学方程式(不必写出反应条件)______________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)若混合液中只含两种组分,则所有可能的组合是_____________________________.
(2)若混合液中含有三种组分,在628 g混和液中有1 mol H2O则混合液中乙醇的物质的量为__________mol.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)写出乙硫醇(C2H5SH)和NaOH反应的化学方程式_____________________________.
(2)写出乙硫醇在O2中完全燃烧的化学方程式__________________________________.
(3)写出乙硫醇和甲酸在一定条件下可发生酯化反应的化学方程式_________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022

(1)烧瓶中液体呈棕黑色的原因____________________________.
(2)一些同学认为:溴水褪色的现象不能证明反应中有乙烯生成,且乙烯具有不饱和性,因为棕黑色物质会与浓H2SO4反应生成某气体,该气体使溴水褪色的反应方程式为_______
_______.
另一些同学经过细致观察后认为:试管中另一现象可证明反应中有乙烯生成且乙烯具有不饱和性.这个现象是_________________________.
(3)为了控制烧瓶中液体的温度,该小组改用图装置实验时,先将烧瓶置于润滑油(沸点、燃点均高于300℃)中然后加热,并控制在170℃左右.结果试管中溴水未完全褪色,液面上形成一层深红棕色液体.产生这个现象的原因是烧瓶中发生反应生成液体X,其反应方程式为______________________________________.
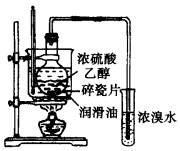
若利用上图制较多的乙烯,正确的加热操作顺序是先_____________________________
_____________________后_________________________________.
(4)处理上述实验后烧瓶中废液的正确操作是________.
A.废液倒入下水道
B.废液倒入空废液缸中
C.将水倒入烧瓶中
D.废液倒入盛水的塑料桶中
查看答案和解析>>
科目: 来源:物理教研室 题型:022
|
物质 |
丙酮 |
乙酸乙酯 |
乙醇 |
乙酸 |
|
沸点(℃) |
56.2 |
77.06 |
78 |
117.9 |
①向废液中加入烧碱溶液,调节pH为10;
②将混合液加入蒸馏器中缓缓加热;
③收集温度在70~85℃时馏出物;
④排出蒸馏器中的残液,冷却后,向其中加浓H2SO4(过量),然后再放入耐酸蒸馏器中进行蒸馏)回收馏出物.据此回答下列问题:
(1)加入烧碱溶液调节pH为10的目的是________________________________.
(2)在70~85℃时馏出物的主要成分是________________________________.
(3)在步骤④中,加入过量浓H2SO4的目的是(用化学方程式表示)__________________
______回收馏出物的温度控制在85~125℃,这时残留液中的主要成分是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com