
科目: 来源: 题型:022
按要求填空:
(1)用已准确称量的 固体配制
固体配制 溶液100mL,所需的仪器为__________.
溶液100mL,所需的仪器为__________.
(2)除去 固体中混有的少量
固体中混有的少量 ,所进行的实验操作依次为:___________、蒸发、结晶__________.
,所进行的实验操作依次为:___________、蒸发、结晶__________.
(3)除去KCl溶液中的 离子,依次加入的溶液为(填溶质的化学式):
离子,依次加入的溶液为(填溶质的化学式):
______________________________________.
查看答案和解析>>
科目: 来源: 题型:022
用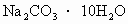 配制
配制 的溶液250mL.
的溶液250mL.
(1)需要使用的主要仪器有_________.
(2)根据计算需称取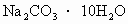 _______________g.
_______________g.
(3)配制溶液有下列几步操作:a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.向容量瓶转移溶液,g.贴标签,h.定容.正确的操作顺序是(填写序号):_________.
(4)下列操作对所配溶液的浓度有何影响(填“偏高”、“偏低”或“无影响”).
①碳酸钠晶体失去了部分结晶水.
②误用“左码右物”的称量方法称量晶体,并动用了游码.
③碳酸钠晶体不纯,含少量NaCl.
④称碳酸钠晶体时所用砝码有锈.
⑤容量瓶未经干燥就进行配制.
⑥向容量瓶转移时,溶液有少量溅出.
⑦定容后,振荡摇匀,静置,发现液面低于刻度线.
⑧没有洗烧杯.
⑨定容时俯视刻度线.
⑩定容时仰视刻度线.
其中引起偏高的有(填序号)________,偏低的有________,无影响的有________.
查看答案和解析>>
科目: 来源: 题型:022
欲用98%的浓硫酸 配制成浓度为
配制成浓度为 的稀硫酸1000mL.简要回答下列问题:
的稀硫酸1000mL.简要回答下列问题:
(1)所需浓硫酸的体积为___________mL.
(2)如果实验室有15mL、20mL、50mL的量筒应选用_________mL的量筒最好,量取时发现量筒不干净用水洗净后直接量取将使结果浓度_________(偏高、偏低、无影响).
(3)将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并不断搅拌的目的是_________,若搅拌过程中有液体溅出结果会使浓度偏_______.
(4)在转入容量瓶前烧杯中液体应________,否则会使结果浓度偏______;并洗涤烧杯2~3次,洗涤液也要转入容量瓶,否则会使结果浓度________.
(5)定容时必须使溶液凹液面与刻度相平,若俯视会使结果浓度______;仰视则使结果浓度____________.
查看答案和解析>>
科目: 来源: 题型:022
有 、
、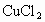 的混合溶液400mL,经测是其中
的混合溶液400mL,经测是其中 是amol/L,向其中投入bg锌粉(过量),充分反应后,过滤.所得滤渣的质量为cg.
是amol/L,向其中投入bg锌粉(过量),充分反应后,过滤.所得滤渣的质量为cg.
(1)求原混合溶液中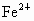 、
、 的物质的量浓度.
的物质的量浓度.
(2)b的数值范围是___________(用含a的代数式表示).
(3)c的数值越大,说明原混合溶液中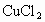 的含量___________(填“越大”、“越小、”),c的最小值应为_________(用含a、b的代数式表示).
的含量___________(填“越大”、“越小、”),c的最小值应为_________(用含a、b的代数式表示).
查看答案和解析>>
科目: 来源: 题型:022
(1)在制取氢氧化亚铁时,要用新制备的硫酸亚铁溶液,其原因是_________,还要将吸有氢氧化钠溶液的胶头滴管插入到硫酸亚铁溶液液面以下,逐滴滴入氢氧化钠溶液,其原因是__________.
(2)100mL容量瓶内装有100mL0.1010mol/L的氯化钠水溶液,设法把它配成0.1000mol/L的氯化钠水溶液可供选用的仪器和用品是:100mL容量瓶(内装上述溶液)、1mL刻度试管、胶头滴管、100mL烧杯、100mL量筒、蒸馏水.
答:______________________________________________.
查看答案和解析>>
科目: 来源: 题型:022
在三个密闭容器中分别装有① 和
和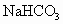 ;②
;② 和
和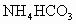 ;③
;③ 和
和 ,其中每种物质均为1mol,将它们加热到300℃经充分反应后排出气体写出各容器内残留固体的分子式及其物质的量.①___________,②___________,③___________.
,其中每种物质均为1mol,将它们加热到300℃经充分反应后排出气体写出各容器内残留固体的分子式及其物质的量.①___________,②___________,③___________.
如果分别加入相同的物质的量浓度的稀硫酸与残留物完全反应,则消耗硫酸溶液的体积由大到小的顺序依次为(用①、②、③表示之)___________________.
查看答案和解析>>
科目: 来源: 题型:022
实验室用浓盐酸配制 的盐酸溶液:
的盐酸溶液:
(1)配制盐酸溶液需要浓盐酸(密度为 ,质量分数为36.5%)的体积为___________.
,质量分数为36.5%)的体积为___________.
(2)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)____________.
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用量筒量取所需的浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
K.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2—3cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是_________________.
查看答案和解析>>
科目: 来源: 题型:022
已知某温度时饱和NaOH溶液中溶质的质量分数为A%,该饱和溶液的密度为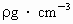 .
.
(1)该溶液中NaOH的物质的量浓度为___________.
(2)该温度下NaOH的溶解度为______.
(3)在100mL水中溶解___________gNaOH,可使溶质的质量分数达到A%,此时溶液的体积为______.
查看答案和解析>>
科目: 来源: 题型:022
(1)甲同学在实验中需要 的NaOH溶液240mL,现实验室中只有容积分别为100mL、250mL、500mL三种容量瓶,他应该选用__________容量瓶.
的NaOH溶液240mL,现实验室中只有容积分别为100mL、250mL、500mL三种容量瓶,他应该选用__________容量瓶.
经计算并正确地称量了NaOH固体后,其后续操作如下:
a.将NaOH固体放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌溶解;
b.待溶液冷却至室温后,转移至未经干燥的容量瓶中;
c.向容量瓶中加蒸馏水直到离刻度线1~2cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切;
d.盖好瓶塞,反复上下颠倒,摇匀.
上述实验操作过程中有一处明显的错误,请用语言叙述并指出对所配溶液浓度的影响___________.
(2)乙同学在实验中需用浓度约为 的NaOH溶液50mL,现实验室中有浓度为
的NaOH溶液50mL,现实验室中有浓度为 的NaOH溶液和蒸馏水,实验仪器只有量筒、烧杯和玻璃棒,无容量瓶.考虑到实验室的实际情况,请你简要描述他应该如何配制:_________.
的NaOH溶液和蒸馏水,实验仪器只有量筒、烧杯和玻璃棒,无容量瓶.考虑到实验室的实际情况,请你简要描述他应该如何配制:_________.
查看答案和解析>>
科目: 来源: 题型:022
有一瓶质量分数为14%的KOH溶液,加热蒸发掉100g水后,得到质量分数为28%的KOH溶液80mL.求所得溶液中KOH的物质的量浓度为_______![]() .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com