
科目: 来源: 题型:022
A、B、C三种元素为短周期元素.A元素的阴离子不能被任何氧化剂氧化,则A离子的电子式为________.1molB单质能从盐酸中置换3g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B离子的结构示意图为________,B的最高价氧化物对应的水化物的化学式为________.C元素有3个电子层,且最外电子层比次外电子层少2个电子,则C元素是________,C与钠反应生成的化合物中的化学键类型是________,该化合物的形成过程是(用电子式表示)________.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:022
已知30℃时几种盐的溶解度:

1862年比利时的索尔维以CO2、NH3、水为原料制得纯净的Na2CO3,叫索尔维法.其主要操作是:①在氨化饱和NaCl溶液中通入CO2制得小苏打;②再把小苏打焙烧,制得纯碱,CO2循环使用;③在析出小苏打的母液中加入生石灰,NH3循环使用.
1943年我国著名科学家侯德榜先生,冲破了“索尔维法”的技术封锁,并加以改进,用固体NaCl代替生石灰加入母液中,使NH4Cl晶体析出,生产纯碱和NH4Cl,这便是举世闻名的“侯氏制碱法”.
(1)写出在氨化饱和NaCl溶液中通入CO2的化学方程式________,该方法能制得小苏打的原因是________.
(2)不能在NaCl溶液中先通入CO2,然后再通入NH3制得NaHCO3的原因是________.
(3)在析出小苏打后的母液中加入生石灰发生反应的化学方程式为________.
(4)“两法”相比,侯氏制碱法的优点是________.
查看答案和解析>>
科目: 来源: 题型:022
氮化钠( )是一种重要的化合物,它与水反应可产生
)是一种重要的化合物,它与水反应可产生 .请回答下列问题:
.请回答下列问题:
(1)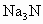 的电子式是________,该化合物是由________键形成.
的电子式是________,该化合物是由________键形成.
(2)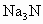 与盐酸反应生成________种盐,其电子式是________.
与盐酸反应生成________种盐,其电子式是________.
(3)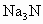 与水的反应属于________反应.
与水的反应属于________反应.
(4)比较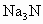 中两种微粒的半径:
中两种微粒的半径: ________
________ (填写“<”、“=”、“>”).
(填写“<”、“=”、“>”).
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:022
Na2O2几乎能与所有的常见气态非金属氧化物反应,如:2Na2O2+2CO2=2Na2CO3+O2↑;Na2O2+CO=Na2CO3,回答下列问题:
(1)写出Na2O2与SO3及SO2反应的化学方程式________.
(2)通过比较可知:当非金属元素处于________价态时,其氧化物与Na2O2反应方生成O2.
查看答案和解析>>
科目: 来源: 题型:022
(1)下列五种物质中①Ne,② ,③
,③ ,④KOH,⑤
,④KOH,⑤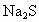 ,只存在共价键的是______,只存在离子键的是______,既存在离子键又存在共价键的是______;不存在化学键的是______.(填写序号).
,只存在共价键的是______,只存在离子键的是______,既存在离子键又存在共价键的是______;不存在化学键的是______.(填写序号).
(2)在下列变化中,①硫的升华,②烧碱熔化,③NaCl溶于水,④HCl溶于水,⑤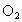 溶于水,⑥
溶于水,⑥ 溶于水,未发生化学键破坏的是______;仅发生离子键破坏的是______;仅发生共价键破坏的是______;既发生离子键破坏,又发生共价键破坏的是______.
溶于水,未发生化学键破坏的是______;仅发生离子键破坏的是______;仅发生共价键破坏的是______;既发生离子键破坏,又发生共价键破坏的是______.
查看答案和解析>>
科目: 来源: 题型:022
甲、乙、丙、丁为前三周期元素形成的微粒,它们的电子总数相等.已知甲、乙、丙为双原子分子或负二价双原子阴离子,丁为原子.
(1)丙与钙离子组成的离子化合物跟水反应产生一种可燃性气体,反应的化学方程式是______.
(2)乙在高温时是一种还原剂,请用化学方程式表示它在工业上的一种重要用途:______.
(3)在一定条件下,甲与 反应的化学方程式是______.
反应的化学方程式是______.
(4)丁的元素符号是______,它的原子结构示意图为________.
(5)丁的氧化物的晶体结构与______的晶体结构相似.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:022
碱金属能形成离子型氢化物.如氢化钠的化学式为NaH,其中H-具有较强的还原性.
(1)常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为________.
(2)NaH能与水剧烈反应生成对应的碱和氢气,反应的化学方程式为________,并在化学方程式中标明电子的转移方向和数目.该反应中氧化产物和还原产物的质量比为________.
查看答案和解析>>
科目: 来源: 题型:022
有A、B、C、D四种元素,A的+2价离子与氩原子的电子层结构相同,B原子有三个电子层,其单质为双原子分子.C的核外电子比A少一个,D与B同周期,其单质为淡黄色固体.
(1)写出A、B、C、D的离子符号:__________.
(2)A、B、C、D的离子半径由小到大的顺序是:_______________________.
(3)用电子式表示这四种元素中两两形成离子化合物的过程.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:022
将一小粒金属钠投入装有CuSO4溶液的烧杯中,产生的现象是________,反应的化学方程式是________.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:022
分析下列氧化还原反应中化合价变化的关系,标出电子转移方向和数目,并指出氧化剂和还原剂.
(1)C+O2 CO2氧化剂________,还原剂________;
CO2氧化剂________,还原剂________;
(2)Cl2+2NaOH=NaCl+NaClO+H2O氧化剂________,还原剂________;
(3)S+2KNO3+3C=K2S+N2+3CO2氧化剂________,还原剂________;
(4)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O氧化剂________,还原剂________.
MnCl2+Cl2↑+2H2O氧化剂________,还原剂________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com