
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
现有A、B、C、D4种元素,A元素形成的-2价阴离子比氦的核外电子数多8个;B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质;C为原子核内有12个中子的二价金属,当2.4g C与足量热水反应时,在标准状况下放出氢气2.24L;D的M层有7个电子.
(1)写出A、B、C、D4种元素的符号:________、________、________、________.
(2)写出B、C、D最高价氧化物的水化物的化学式:________、________、________,并比较其酸碱性:________.
(3)D的气态氢化物为________,D的气态氢化物与 、HF的稳定性由强到弱的顺序为________.
、HF的稳定性由强到弱的顺序为________.
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
A、B、C、D为周期表上36号以前的元素,原子半径A<B,A是周期表中未成对电子数最多的元素,A、B同族,B、C同周期,D与A、B、C三元素既不同周期也不同族,C、D可形成离子化合物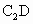 ,且两离子具有相同的电子层结构.请回答下列问题:
,且两离子具有相同的电子层结构.请回答下列问题:
(1)A原子的电子式:________
(2)B原子的原子结构示意图:________
(3)用电子式表示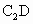 的形成过程:________
的形成过程:________
(4)B、D可形成 ,此化合物能被浓
,此化合物能被浓 氧化,元素B和D均变成各自的最高价氧化物的水化物,同时有红棕色的气体
氧化,元素B和D均变成各自的最高价氧化物的水化物,同时有红棕色的气体 产生,该反应的化学方程式是:________
产生,该反应的化学方程式是:________
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
A、B、C、D都是短周期元素.A元素最高化合价为+5价,B的最高价含氧酸的化学式是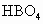 ,C的阳离子和D的阴离子具有相同的电子层结构,D和B在同一主族,D和A在同一周期,1mol C的单质和足量盐酸反应可产生11.2L气体(标准状况).
,C的阳离子和D的阴离子具有相同的电子层结构,D和B在同一主族,D和A在同一周期,1mol C的单质和足量盐酸反应可产生11.2L气体(标准状况).
回答下列问题:
(1)这四种元素的元素符号是:A________,B________,C________,D________.
(2)C和D形成的化合物的化学式是________.
(3)写出C的单质和稀盐酸反应的离子方程式:________
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
处于相邻两个周期的主族元素A、B、C、D,它们的原子半径依次变小.A离子和B离子相差两个电子层,且能形成 型离子化合物.C的离子带3个正电荷.D的气态氢化物通式为
型离子化合物.C的离子带3个正电荷.D的气态氢化物通式为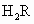 ,在最高价氧化物中,D含量为40%,D的原子序数大致等于其相对原子质量数值的一半.试回答(写名称、符号):
,在最高价氧化物中,D含量为40%,D的原子序数大致等于其相对原子质量数值的一半.试回答(写名称、符号):
(1)A是________元素,在周期表的位置________;
B是________元素,在周期表的位置________;
C是________元素,在周期表的位置________;
D是________元素,在周期表的位置________.
(2)B、C、D单质的还原性从大到小的顺序是________.
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
A、B、C、D、E是相邻三个周期的五种元素,它们的原子序数依次增大.B、C、D在同一周期中,A、E处于同一主族.已知:①除A外各元素原子内层均已填满电子,其中B原子的最外层电子数是其电子层数的2倍;②在A与B形成的化合物中,A占25%;③B与C形成 型化合物;④D与E形成离子化合物,其中阴、阳离子的电子层结构相同.
型化合物;④D与E形成离子化合物,其中阴、阳离子的电子层结构相同.
(1)写出各元素的元素符号:A________,B________,C________,D________,E________.
(2)其中原子半径最大的原子是________,吸引电子能力最强的原子是________.
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
短周期元素X、Y、Z在周期表中的位置关系如图所示,试回答:

(1)X元素名称是________,Z元素符号是________,Z元素最高价氧化物对应水化物的化学式是________.Z元素的非金属性比氯元素强还是弱?________其原子半径比氯原子的原子半径大还是小?________,判断根据是________.
(2)Y元素是________,Y元素形成的单质通入水中反应的化学方程式是:________
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20.其中X、Z是金属元素;V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半.由此推知(填元素符号):V是________,W是________,X是________,Y是________,Z是________.
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
有两种气态单质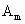 和
和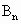 ,已知2.4g
,已知2.4g 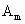 和2.1g
和2.1g 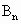 所含的原子个数相等,而分子数之比却为2∶3,A和B的原子核内质子数都等于中子数,A原子L层电子数是K层电子数的3倍.
所含的原子个数相等,而分子数之比却为2∶3,A和B的原子核内质子数都等于中子数,A原子L层电子数是K层电子数的3倍.
(1)A、B各是什么元素?A________,B________.
(2)![]() 中m值是________.
中m值是________. 的同素异形体是
;
的同素异形体是
;
(3)B的气态氢化物与B的最高价氧化物的对应水化物反应生成的化合物的化学式为
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
写出下列粒子的化学式:
(1)由2个原子组成,含有18个电子的分子是________.
(2)由3个原子组成,含有18个电子的分子是________.
(3)由4个原子组成,含有18个电子的分子是________.
(4)由5个原子组成,含有18个电子的分子是________.
查看答案和解析>>
科目: 来源:黄冈重点作业 高一化学(下) 题型:022
某核素R具有微弱放射性,其原子核内的中子数比质子数多43,由它组成的固体单质A,在一定条件下密度为6.88g· ,用X射线研究其固体表明,在边长为1.00×
,用X射线研究其固体表明,在边长为1.00× 的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中
的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中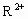 稳定,而
稳定,而 有强氧化性,可将NO氧化为
有强氧化性,可将NO氧化为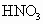 .氧化物
.氧化物 ,其性质与
,其性质与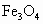 有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途.
有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途.
请回答:
(1)R原子的摩尔质量为________.
(2)R元素处于周期表中第________周期________族.
(3)假若把少量 加到
加到 溶液中,是否会发生反应?
溶液中,是否会发生反应?
若“否”,其原因为:________.
若“是”,其离子反应方程式为:________
(4) 因具有氧化性,而大量用于油漆涂料,涂在钢铁表面,有利于形成耐腐蚀的钝化层.
因具有氧化性,而大量用于油漆涂料,涂在钢铁表面,有利于形成耐腐蚀的钝化层. 与足量的
与足量的 反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.
反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com